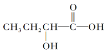��Ŀ����
����Ŀ�������仯�����ڹ�ҵ������Ҫ��;����ش������й����⣺
��1����֪N2(g)+O2(g)=2NO(g) ��H =+180.5kJ��mol��1��N2(g)+3H2(g) ![]() 2NH3(g)��H =��92.4kJ��mol��1��2H2(g)+O2(g)=2H2O(g) ��H =��483.6kJ��mol��1��д����������������ȫ����һ��������ˮ�������Ȼ�ѧ����ʽΪ_________
2NH3(g)��H =��92.4kJ��mol��1��2H2(g)+O2(g)=2H2O(g) ��H =��483.6kJ��mol��1��д����������������ȫ����һ��������ˮ�������Ȼ�ѧ����ʽΪ_________
��2����һ��������ܱ������У��������»�ѧ��Ӧ��N2(g)+3H2(g) ![]() 2NH3(g)���ں��º�ѹ���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������______(�����)��
2NH3(g)���ں��º�ѹ���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������______(�����)��
A��2v(H2)(��)=3v(NH3)(��) B��2v(N2) (��)=v(H2) (��)
C��������ѹǿ���ֲ��� D�����������ܶȱ��ֲ���
��3�������������£����ʹ���M�ܴ�![]() ��
��![]() ����
����![]() ����һ��������
����һ��������![]() ��
��![]() ��
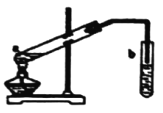
��![]() �Ļ�����壬����ͨ��װ�д���M�ķ�Ӧ���з�Ӧ��װ�ü�ͼ����
�Ļ�����壬����ͨ��װ�д���M�ķ�Ӧ���з�Ӧ��װ�ü�ͼ����
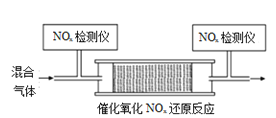
��Ӧ��ͬʱ��![]() ��ȥ�����淴Ӧ�¶ȵı仯������ͼ��ʾ����
��ȥ�����淴Ӧ�¶ȵı仯������ͼ��ʾ����![]() ��Χ�������¶ȵ����ߣ�
��Χ�������¶ȵ����ߣ�![]() ��ȥ������Ѹ������������������Ѹ���������Ǵ����������¶������������¶����߹�ͬʹ
��ȥ������Ѹ������������������Ѹ���������Ǵ����������¶������������¶����߹�ͬʹ![]() ȥ����Ӧ����Ѹ�����������λ�����Ҫ��____________������Ӧ�¶ȸ���
ȥ����Ӧ����Ѹ�����������λ�����Ҫ��____________������Ӧ�¶ȸ���![]() ʱ��
ʱ��![]() ��ȥ����Ѹ���½���ԭ�������_________��
��ȥ����Ѹ���½���ԭ�������_________��
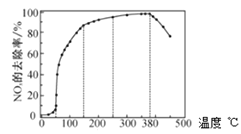
��4����ͼΪ������![]() ������ȼ�ϵ�ص������ͭ��Һ��ʾ��ͼ��
������ȼ�ϵ�ص������ͭ��Һ��ʾ��ͼ��
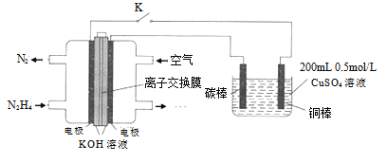
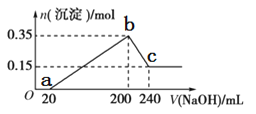
��ͼ������ӦʽΪ��___________������ͼ�����Ϸų�2.24L����![]() ��״��
��״��![]() ʱ��ͼ������ͭ��Һ��pH=______(��Һ����仯���Բ��ƣ���
ʱ��ͼ������ͭ��Һ��pH=______(��Һ����仯���Բ��ƣ���
��4����ҵ���������صĻ�ѧ����ʽΪ��2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(l)����T�棬���Ϊ4L���ܱ������У�ͨ��6mol NH3��3mol CO2 ��10min��Ӧ�ﵽƽ�⣬�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1����10min�ڵ�ƽ����Ӧ������(CO2)��_______mol��L��1��min��1������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3mol NH3�����ʱ��Ӧ��v��____ v��(����>����<������=��)��
CO(NH2)2(s)+H2O(l)����T�棬���Ϊ4L���ܱ������У�ͨ��6mol NH3��3mol CO2 ��10min��Ӧ�ﵽƽ�⣬�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1����10min�ڵ�ƽ����Ӧ������(CO2)��_______mol��L��1��min��1������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3mol NH3�����ʱ��Ӧ��v��____ v��(����>����<������=��)��
���𰸡�4NH3(g)+5O2(g)=4NO(g)+6H2O(g)��H=905.0kJ/mol AC Ѹ���������Ǵ����������¶������������¶����߹�ͬʹNOxȥ����Ӧ����Ѹ������ �����λ�����Ҫ���¶����������NOxȥ����Ӧ���������Ǵ��������½��������ڸ���������������Ӧ����NO N2H44e+4OH��N2��+4H2O PH=0 0.05 <
��������
��1��������֪�Ȼ�ѧ����ʽ��˹���ɼ��㣬�ɸ�˹���ɢ���2-����2+����3�õõ���Ӧ���ʱ䣬д����Ӧ��Ӧ���Ȼ�ѧ����ʽ��
��2������ƽ��״̬���ж������жϣ�ƽ���־�����������������Ӧ���ʵ����淴Ӧ���ʣ���Ӧ������и���ֵĺ������ֲ��䣮
��3����һ���¶ȷ�Χ�ڴ������Խϴ������¶ȷ�Χ���������Խ��ͣ����¶ȡ����������£������ܱ�����������NO��
��4����N2H4ȼ�ϵ�ص������ͭ��Һ��װ����ͼ��ʾ�����Ϊȼ��ԭ���װ�ã�ͨ��N2H4�ĵ缫Ϊ������N2H4ʧ���ӷ���������Ӧ����ӦʽΪN2H44e+4OH��N2��+4H2O��ͨ������ĵ缫Ϊ�����������õ��ӷ�����ԭ��Ӧ����ӦʽΪO2+2H2O+4e=4OH���ұ�Ϊ���أ��븺��������ͭΪ��������Ӧʽ��Cu2++2e=Cu����2H++2e=H2������̼���缫������Ϊ��������Ӧʽ2H2O4e=4H++O2�����ݴ˷�����
��5��2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(l)�����ð���Ũ�ȵı仯��������������ʣ����ð����Ͷ�����̼������֮�����������֮�ȣ������������̼�����ʣ�����ƽ�ⳣ�����㣬Ũ����QC��K�Ĺ�ϵ�жϷ�Ӧ����
CO(NH2)2(s)+H2O(l)�����ð���Ũ�ȵı仯��������������ʣ����ð����Ͷ�����̼������֮�����������֮�ȣ������������̼�����ʣ�����ƽ�ⳣ�����㣬Ũ����QC��K�Ĺ�ϵ�жϷ�Ӧ����
(1)��֪N2(g)+O2(g)�T2NO(g)��H=+180.5kJ/mol��N2(g)+3H2(g)�T2NH3(g)��H=92.4kJ/mol��2H2(g)+O2(g)�T2H2O(g)��H=483.6kJ/mol�ۣ��ɸ�˹���ɢ���2����2+����3�ã�4NH3(g)+5O2(g)�T4NO(g)+6H2O(g)��H=905.0kJ/mol���ʴ�Ϊ��4NH3(g)+5O2(g)=4NO(g)+6H2O(g)��H=905.0kJ/mol��
(2)A. ��ͬ���ʵ����淴Ӧ����֮�ȵ����������֮����ƽ��״̬����֤�����淴Ӧ������ȣ���A��ȷ��
B. ��ͬ���ʵ����淴Ӧ����֮�ȵ����������֮����ƽ��״̬��2v(N2)(��)=v(H2)(��)����ƽ��״̬����B����
C. ������ѹǿ���䣬��������ʵ������䣬�÷�Ӧ��ƽ��״̬����C��ȷ��
D. ��������ܱ������з�Ӧ���������䣬������䣬�ܶ�ʼ�ղ��䣬��D����
AC��ȷ���ʴ�ѡ��AC��
��3����һ���¶ȷ�Χ�ڴ������Խϴ������¶ȷ�Χ���������Խ��ͣ�����ͼ֪��
Ѹ���������Ǵ����������¶������������¶����߹�ͬʹNOxȥ����Ӧ����Ѹ�����������λ�����Ҫ���¶����������NOxȥ����Ӧ���������Ǵ��������½������¶ȡ����������£������ܱ�����������NO������Ӧ�¶ȸ���380��ʱ��NOx��ȥ����Ѹ���½���ԭ������ǰ����ڸ���������������Ӧ����NO���ʴ�Ϊ��Ѹ���������Ǵ����������¶������������¶����߹�ͬʹNOxȥ����Ӧ����Ѹ�����������λ�����Ҫ���¶����������NOxȥ����Ӧ���������Ǵ��������½��������ڸ���������������Ӧ����NO��
��4��ͨ��N2H4�ĵ缫Ϊ������N2H4ʧ���ӷ���������Ӧ��1��N2H4ʧȥ4�����ӣ���ӦʽΪN2H44e+4OH��N2��+4H2O���븺��������ͭΪ�������缫��Ӧʽ��Cu2++2e=Cu����2H++2e=H2��������������µ�����2.24L������Ϊ�����������ʵ���Ϊn=![]() =
=![]() =0.1mol������ת�Ƶ����������������ʵ���֮��Ϊ2:1���ڶ���ת�Ƶĵ��ӵ����ʵ���Ϊ0.2mol����һ��ת�Ƶĵ��ӵ����ʵ���ҲΪ0.2mol����ת��0.4mol���ӣ���һ���ܷ�ӦΪ2CuSO4+2H2O= 2Cu+O2+2H2SO4���ڶ�����Ϊ���ˮ��ת��4mol��������2mol���ᣬ��ת��0.2mol����������������ʵ���Ϊ0.1mol�������������ӵ����ʵ���Ϊ0.2mol�������ӵ�Ũ��Ϊ
=0.1mol������ת�Ƶ����������������ʵ���֮��Ϊ2:1���ڶ���ת�Ƶĵ��ӵ����ʵ���Ϊ0.2mol����һ��ת�Ƶĵ��ӵ����ʵ���ҲΪ0.2mol����ת��0.4mol���ӣ���һ���ܷ�ӦΪ2CuSO4+2H2O= 2Cu+O2+2H2SO4���ڶ�����Ϊ���ˮ��ת��4mol��������2mol���ᣬ��ת��0.2mol����������������ʵ���Ϊ0.1mol�������������ӵ����ʵ���Ϊ0.2mol�������ӵ�Ũ��Ϊ![]() =
=![]() =1mol/L��PH=0���ʴ�Ϊ��N2H44e+4OH��N2��+4H2O��PH=0��
=1mol/L��PH=0���ʴ�Ϊ��N2H44e+4OH��N2��+4H2O��PH=0��
��5����ʼ״̬6mol NH3��3mol CO2�����Ϊ4L����Ũ��Ϊc(NH3)=![]() =
=![]() =1.5mol/L��c(CO2)=
=1.5mol/L��c(CO2)=![]() =
=![]() =0.75mol/L��10min��Ӧ�ﵽƽ�⣬�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1��v(NH3)=
=0.75mol/L��10min��Ӧ�ﵽƽ�⣬�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1��v(NH3)=![]() =
=![]() =0.1mol/(L��min)�����ڰ����������̼������֮�ȵ��ڻ�ѧ����ʱ֮�ȣ���v(CO2)=
=0.1mol/(L��min)�����ڰ����������̼������֮�ȵ��ڻ�ѧ����ʱ֮�ȣ���v(CO2)=![]() v(NH3)=0.5��0.1mol/(L��min)=0.05 mol/(L��min)�������⽨����������ʽ��
v(NH3)=0.5��0.1mol/(L��min)=0.05 mol/(L��min)�������⽨����������ʽ��
2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(l)
CO(NH2)2(s)+H2O(l)
��ʼ(mol/L) 1.5 0.75
�仯(mol/L) 1.0 0.5
ƽ��(mol/L) 0.5 0.25
�¶Ȳ��䣬ƽ�ⳣ�����䣬ƽ��ʱc(NH3)=0.5molL1��c(CO2)=0.25molL1����Ӧ��ƽ�ⳣ��K=![]() =
=![]() =16��ͬ��ͬѹ�£�����ȵ������ʵ���֮�ȣ�����ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3molNH3���������ΪVL����
=16��ͬ��ͬѹ�£�����ȵ������ʵ���֮�ȣ�����ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3molNH3���������ΪVL����![]() =
=![]() ����ã�V=8L����ʱQc=
����ã�V=8L����ʱQc=![]() =
=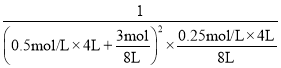 =20.48>16=K��˵����ʱƽ�����������ƶ�����V��<V�����ʴ�Ϊ��0.05��<��
=20.48>16=K��˵����ʱƽ�����������ƶ�����V��<V�����ʴ�Ϊ��0.05��<��

 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�����Ŀ����֪A--F�����л�����������Ҫ���л��ϳ�ԭ�ϣ��ṹ��ʽ���±��������Ҫ��ش��������⣺
������ | A | B | C |
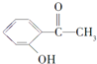
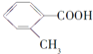
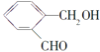
�ṹ��ʽ |
|
|
|
������ | D | E | F |
�ṹ��ʽ |
|
|
|
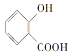
![]() д����������������A��ͬ���칹��Ľṹ��ʽ�� ______ ��
д����������������A��ͬ���칹��Ľṹ��ʽ�� ______ ��
A.�˴Ź���������4���
B.�ܷ���ˮ�ⷴӦ
C.�ڼ����������ܹ������Ƶ�������ͭ����Һ����ש��ɫ����
![]() ������B����ȡ������ʧ��ҩ��--��������м��壬�����й���������ȷ����______
������B����ȡ������ʧ��ҩ��--��������м��壬�����й���������ȷ����______ ![]() ����ĸ
����ĸ![]() ��
��
A.�����Ȼ�����Һ��ɫ![]() �����к����Ȼ����ǻ��ȹ�����
�����к����Ȼ����ǻ��ȹ�����
C.������ˮ��Ӧ![]() ����̼������Һ��Ӧ����������̼
����̼������Һ��Ӧ����������̼
![]() ������B��һ�������£�������NaOH��Һ������Ӧ����1mol������B�����ҪNaOH�����ʵ���Ϊ ______ ��
������B��һ�������£�������NaOH��Һ������Ӧ����1mol������B�����ҪNaOH�����ʵ���Ϊ ______ ��
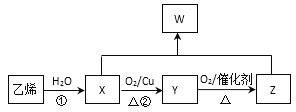
![]() ������C��D��һ�������·�������ת���õ��߷��ӻ�����Z�����ֲ�������ȥ��
������C��D��һ�������·�������ת���õ��߷��ӻ�����Z�����ֲ�������ȥ��
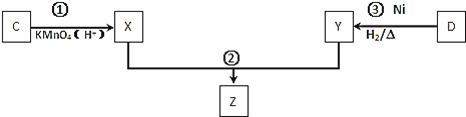
��Ӧ![]() ��D��
��D��![]() �����ʵ���1��1��Ӧ����Y����Ӧ
�����ʵ���1��1��Ӧ����Y����Ӧ![]() �Ļ�ѧ����ʽΪ ______ ��
�Ļ�ѧ����ʽΪ ______ ��
![]() ������D��������Һ��Ӧ�Ļ�ѧ����ʽ
������D��������Һ��Ӧ�Ļ�ѧ����ʽ![]() �л����ýṹ��ʽ��ʾ
�л����ýṹ��ʽ��ʾ![]() �� ______ ��
�� ______ ��
![]() ������F�Ǻϳɿ���ƽ��ԭ��֮һ��
������F�Ǻϳɿ���ƽ��ԭ��֮һ��![]() ����ƽ��һ���������β���ҩ��
����ƽ��һ���������β���ҩ��![]() ����ϳ�·������
����ϳ�·������![]() ��Ӧ����һ�������½���
��Ӧ����һ�������½���![]() ��
��

![]() ��Ӧ
��Ӧ![]() ��ԭ��������
��ԭ��������![]() �ķ�Ӧ����÷�Ӧ�Ļ�ѧ����ʽΪ ______ ��
�ķ�Ӧ����÷�Ӧ�Ļ�ѧ����ʽΪ ______ ��
![]() ����ת����ϵ��û���漰�ķ�Ӧ������ ______
����ת����ϵ��û���漰�ķ�Ӧ������ ______ ![]() �����
�����![]() ��
��
![]() �ӳɷ�Ӧ
�ӳɷ�Ӧ![]() ��ȥ��Ӧ
��ȥ��Ӧ![]() ��ԭ��Ӧ
��ԭ��Ӧ![]() ������Ӧ
������Ӧ![]() �Ӿ۷�Ӧ
�Ӿ۷�Ӧ![]() ȡ����Ӧ��
ȡ����Ӧ��