题目内容
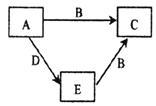
【题目】如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1。B为___极,A极的电极反应为___。
(2)打开K1,合并K2。E为___极,F极的电极反应为___,
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是___,原因是___。
【答案】负 O2+2H2O+4e-=4OH- 阴 2Cl--2e-=Cl2↑ AE 因为A极产生OH-,E极中H+反应了,促进了水的电离,溶液中有OH-剩余,酚酞遇OH-变红
【解析】
(1)当打开K2,闭合K1时,铁片、石墨和NaCl溶液构成原电池,负极为铁,电极反应式为:Fe-2e-═Fe2+,正极为石墨,正极的电极反应式为:O2+4e-+2H2O═4OH-,故答案为:负;O2+4e-+2H2O═4OH-;
(2)当打开K1,闭合K2时,铁片、石墨和NaCl溶液构成电解池,阴极为铁,电极反应式为:2H++2e-═H2↑,阳极为石墨,电极反应式为:2Cl--2e-═Cl2↑,故答案为:阴;2Cl--2e-═Cl2↑;
(3)由于A极O2得到电子产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性,所以A、E电极周围遇酚酞变红,
故答案为:AE;A极上O2放电产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目