题目内容
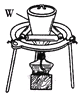
【题目】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如下图所示。

(1)写出下列线段内发生反应的离子方程式:
OD段_________________________,
CD段_________________________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为____________。
(3)图中C点表示当加入_______ mol NaOH时,Al3+已经______,Mg2+已经___________。
(4)图中线段OA∶AB=____________。
【答案】Al3++ 3 OH- === Al(OH)3↓、Mg2++ 2 OH- === Mg(OH)2↓ Al(OH)3+ OH- === AlO2- +2H2O 2∶1 0.8 全部生成NaAlO2 完全生成沉淀Mg(OH)2 7∶1
【解析】
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液,先生成氢氧化铝、氢氧化镁沉淀,再加氢氧化钠,氢氧化铝又逐渐溶解。
⑴OD段是镁离子和铝离子沉淀的阶段,离子方程式为Al3++ 3 OH- === Al(OH)3↓、Mg2++ 2 OH- === Mg(OH)2↓,故答案为:Al3++ 3 OH- === Al(OH)3↓、Mg2++ 2 OH- === Mg(OH)2↓。
CD段是氢氧化铝溶解在氢氧化钠溶液中,离子方程式为Al(OH)3+ OH- === AlO2- +2H2O,故答案为:Al(OH)3+ OH- === AlO2- +2H2O。
(2)通过图像分析,n[Al(OH)3]:n[Mg(OH)2]=1:2,根据元素守恒,原溶液中Mg2+、Al3+的物质的量浓度之比为2:1,故答案为:2:1。
(3)根据图像分析得出图中C点氢氧化铝全部溶解,Al3+全部生成NaAlO2,Mg2+完全生成沉淀Mg(OH)2,C点加入NaOH的物质的量为n(NaOH) = 4n(Al3+)+2n(Mg2+)=4×0.1 mol+2×0.2mol = 0.8 mol,故答案为:0.8;全部生成NaAlO2;完全生成沉淀Mg(OH)2;
(4)根据上题分析得出AB阶段消耗0.8molNaOH,OA阶段消耗氢氧化钠物质的量n(NaOH) = 3n(Al3+)+2n(Mg2+)=3×0.1 mol+2×0.2mol = 0.7 mol,图中线段OA∶AB=7:8,故答案为:7:8。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案