题目内容
5.下列变化中,需加氧化剂才能实现的是( )| A. | C→CO2 | B. | Na2O2→O2 | C. | NaClO→NaCl | D. | CaO→Ca(OH)2 |
分析 需加氧化剂才能实现,则选项中为还原剂的发生的氧化反应,还原剂中某元素的化合价升高,以此来解答.
解答 解;A.C→CO2中C元素的化合价升高,被氧化,需要氧化剂实现,故A正确;
B.Na2O2→O2中Na2O2与水反应即可实现,无需加入还原剂,故B错误;
C.NaClO→NaCl中,Cl元素的化合价降低,需要还原剂实现,故C错误;
D.CaO→Ca(OH)2中,没有元素的化合价变化,不发生氧化还原反应,故D错误.
故选A.
点评 本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应还原剂的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.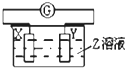 如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的( )
如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的( )
 如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的( )
如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的( )| A. | X是Zn,Y是Cu,Z为稀H2SO4 | B. | X是Cu,Y是Zn,Z为稀H2SO4 | ||
| C. | X是Fe,Y是Ag,Z为稀AgNO3溶液 | D. | X是Ag,Y是Fe,Z为稀AgNO3溶液 |
16.从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作.下列图示对应的装置合理,操作规范的是( )
| A. | 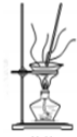 灼烧 | B. | 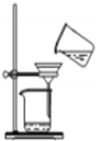 过滤 | ||
| C. |  分液 | D. | 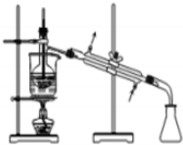 蒸馏 |
13.下列关于卤素及其化合物的叙述错误的是( )
| A. | 非金属性:F>Cl>Br>I | B. | 单质氧化性:F2>Cl2>Br2>I2 | ||
| C. | 氢化物稳定性:HF>HCl>HBr>HI | D. | 沸点:F2>Cl2>Br2>I2 |
20.化学反应的实质是旧键的断裂和新键的生成,在探讨发生反应的分子中化学键在何处断裂的问题时,近代科技常用同位素示踪原子法.如有下列反应: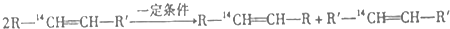
可以推知,化合物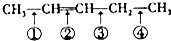 反应时断裂的化学键应是( )
反应时断裂的化学键应是( )
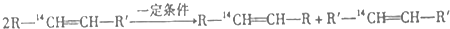
可以推知,化合物
 反应时断裂的化学键应是( )
反应时断裂的化学键应是( )| A. | ①③ | B. | ①④ | C. | ② | D. | ②③ |
10.下列各项中表达正确的是( )
| A. | F-的结构示意图: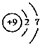 | B. | CO2的分子模型示意图: | ||
| C. | N2的结构式::N≡N: | D. | CSO的电子式: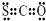 |
14.两种金属混合粉末15g,与足量的盐酸反应时,生成11.2L氢气(标准状况),符合上述的金属混合物是( )
| A. | Mg 和 Ag | B. | Mg和 Al | C. | Cu和 Zn | D. | Fe 和 Zn |
15.下列化学用语正确的是( )
| A. | H2O2的电子式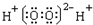 | |
| B. | 甲醛的结构简式:CH2O | |
| C. | N2的结构式::N≡N: | |
| D. | 质子数为53、中子数为72的碘原子:${\;}_{53}^{125}$I |