题目内容
12.某实验小组需要配制230mL 0.01mol/L的NaOH溶液,配制步骤如下:①完全溶解以后,立刻转移入容量瓶中;
②往容量瓶加水至离刻度线2~3厘米处,改用胶头滴管加水至刻度线;
③在托盘天平上,称量0.092g NaOH固体(用小烧杯盛);
④用蒸馏水洗涤烧杯和玻棒,并转移入容量瓶中,洗涤共2次;
⑤往小烧杯中加水溶解,同时用玻棒搅拌;
(1)在上面的横线处填写该操作重要的实验仪器;
(2)正确的配制步骤顺序应该是:③⑤①④②;
(3)在上述配制步骤中,有些地方错误了,请找出错误的步骤序号,并加以改正(可不填满,如有需要,可自行添加):
步骤序号①,改正为完全溶解后,待溶液冷却至室温,再转移入容量瓶.
步骤序号③,改正为电子天平称量0.100g氢氧化钠固体.
步骤序号.,改正为..
(4)下列操作中,哪些操作会使溶液的浓度偏低?ABD
A、摇匀后,液面稍低于刻度线,再加水使之相平;
B、转移时,有少量溶液滴到实验桌上;
C、溶液转移前,容量瓶中已经有少量蒸馏水;
D、定容时,不小心加水超过了刻度线,趁还未摇匀,立刻吸出多余的水.
分析 (1)②定容时,要用胶头滴管加水至刻度线;
③固体的称量用托盘天平;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(3)根据配制步骤方法来分析;
(4)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:(1)②定容时,开始将水直接导入容量瓶至液面离刻度线1-2cm,然后要用胶头滴管加水至凹液面与刻度线相切,故答案为:胶头滴管;
③固体的称量用托盘天平,故答案为:托盘天平;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序为:③⑤①④②,故答案为:③⑤①④②;
(3)由于容量瓶不能受热,故步骤1中应将氢氧化钠溶解后,应将溶液冷却至室温后再移液;
托盘天平只能精确至0.1g,故步骤③中称量0.092g NaOH固体不能用托盘天平,应改用电子天平.
故答案为:①;完全溶解后,待溶液冷却至室温,再转移入容量瓶;③;电子天平称量0.100g 氢氧化钠固体;
(4)A、摇匀后,液面稍低于刻度线是正常的,再加水使之相平会导致溶液的浓度偏低,故A正确;
B、转移时,有少量溶液滴到实验桌上,会导致溶质的损失,则浓度偏低,故B正确;
C、若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,故C错误;
D、定容时,不小心加水超过了刻度线,趁还未摇匀,立刻吸出多余的水,则吸出的水中有溶质,则会导致溶液的浓度偏低,故D正确;
故选ABD.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
3.叶蝉散(isoprocard)对睡到叶蝉和飞虱具有较强的触杀作用,防效迅速,但残效不长.工业上用邻异丙基苯酚合成叶蝉散的过程如下:
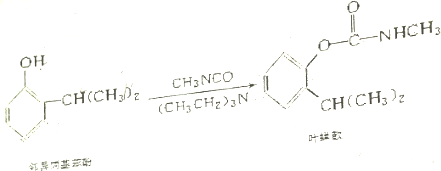
下列有关正确的是( )

下列有关正确的是( )
| A. | 叶蝉散的分子式是C11H16NO2 | |
| B. | 叶蝉散分子不能发生氧化反应 | |
| C. | 邻异丙基苯酚的核磁共振氢谱有7个峰 | |
| D. | 邻异丙基苯酚与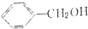 互为同系物 互为同系物 |
20.下列有关气体体积的叙述中,正确的是( )
| A. | 一定温度、压强下,1mol气态物质体积的大小由构成气体的分子大小决定 | |
| B. | 一定温度、压强下,1mol气态物质体积的大小由构成气体的分子间距决定 | |
| C. | 不同的气体,若体积不同,则它们所含的分子数也不同 | |
| D. | 气体摩尔体积是指1 mol任何气体所占的体积约为22.4L |
7.化学知识在生活中有重要意义,下列说法不正确的是( )
| A. | 草木灰(含有K2CO3)水溶液可以用于洗涤油污 | |
| B. | 乙醇、乙酸和甲醛广泛应用于食品加工 | |
| C. | 捕获排放的CO2能降低地球的温室效应 | |
| D. | 反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
2.通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
| A. | 分子中键角小于109.5°是因为氮原子轨道杂化类型为sp2杂化 | |
| B. | Cl的电负性强于N的电负性 | |
| C. | NCl3分子是极性分子 | |
| D. | NBr3 比NCl3易挥发 |
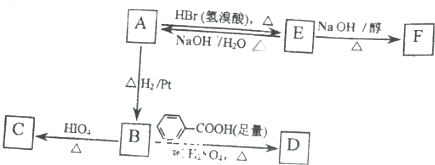
 $→_{△}^{HIO_{4}}$RCHO+R′CHO
$→_{△}^{HIO_{4}}$RCHO+R′CHO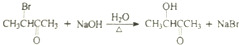 .
. .
. HSO3-+OH-.
HSO3-+OH-.