题目内容
(10分)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属。通常
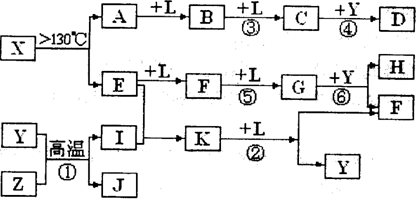
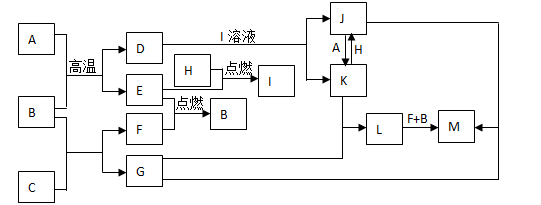
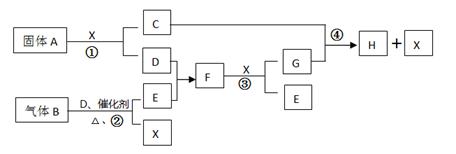
条件下D为无色无味气体,无色气体G遇空气变红棕色。已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。各物质之间的转化关系如下图(部分反应产物已略去)。

请回答下列问题:
(1)A的化学式为 。
(2)A溶液与Na2O2反应的总化学方程式为 。
(3)E的稀溶液与F溶液反应的离子方程式为 。
(4)电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为 。(假设溶液体积不变)
(5)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 。(假设溶液体积不变)
条件下D为无色无味气体,无色气体G遇空气变红棕色。已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。各物质之间的转化关系如下图(部分反应产物已略去)。

请回答下列问题:
(1)A的化学式为 。
(2)A溶液与Na2O2反应的总化学方程式为 。
(3)E的稀溶液与F溶液反应的离子方程式为 。
(4)电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为 。(假设溶液体积不变)
(5)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 。(假设溶液体积不变)
(10分)
(1)Cu(NO3)2
(2)Cu(NO3)2+2Na2O2+2H2O=Cu(OH)2↓+4NaNO3+O2↑
(3)3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
(4)2 (5)0.2mol/L
(1)Cu(NO3)2
(2)Cu(NO3)2+2Na2O2+2H2O=Cu(OH)2↓+4NaNO3+O2↑
(3)3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
(4)2 (5)0.2mol/L
解:(1)电解A溶液时产生金属单质C和另外一种气体D,应为电解含氧酸盐溶液,在阴极上析出不活泼金属,则C应为铜,D为氧气,E溶液能与C金属发生氧化还原反应,且E溶液与F溶液也能反应生成无色无味气体G,说明E溶液具有强氧化性,应为硝酸,故A为硝酸,C为铜,D为氧气,G为NO,F与硝酸反应生成NO,说明且含有金属B元素,说明F溶液具有还原性,应为Fe(NO3)2溶液,B为Fe,H为Fe(NO3)3,故答案为:Cu(NO3)2;
(2)Na2O2与水加入到Cu(NO3)2溶液中反应生成NaOH和氧气,NaOH和Cu(NO3)2反应生成蓝色沉淀2Cu(OH)2,故答案为:2Na2O2+2Cu(NO3)2+2H2O=2Cu(OH)2↓+4NaNO3+O2↑;
(3)硝酸具有强氧化性,Fe2+具有还原性,二者发生氧化还原反应,故答案为:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O;
(4)根据电解硝酸铜的电极方程式:

5)向盐A溶液中加入金属单质B,反应的化学方程式为:Fe+Cu(NO3)2═Fe(NO3)2+Cu,根据差量法计算:

故答案为:0.2 mol/L.

练习册系列答案
相关题目



 。
。 。
。