��Ŀ����
10��X��Y��Z��W�Ƿֱ�λ�ڵ�2��3���ڵ�Ԫ�أ�ԭ���������ε�����X��Zλ��ͬһ���壬YԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ��Zԭ�ӵ������������Ǵ�����������һ�룬Y��Z��Wԭ�ӵ�����������֮��Ϊ14������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��С�����˳��X��Y��Z��W | |
| B�� | Z���������������ˮ��Ӧ������Ӧ���� | |
| C�� | Y������һ�������¿����������������û���Ӧ | |
| D�� | �����£�0.1 mol/L w����̬�⻯���ˮ��Һ��������Ũ��С��0.1 mol/L |
���� X��Y��Z��W�Ƿֱ�λ�ڵ�2��3���ڵ�Ԫ�أ�ԭ���������ε�����YԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ��ӦΪAlԪ�أ�Zԭ�ӵ������������Ǵ�����������һ�룬ӦΪSiԪ�أ�X��Zλ��ͬһ���壬��XΪCԪ�أ�Y��Z��Wԭ�ӵ�����������֮��Ϊ14����W������������Ϊ14-3-4=7����ԭ���������ӦΪClԪ�أ����Ԫ�������ɵĵݱ�����ж�Ԫ�ض�Ӧ�ĵ��ʡ�����������ʣ�
��� �⣺X��Y��Z��W�Ƿֱ�λ�ڵ�2��3���ڵ�Ԫ�أ�ԭ���������ε�����YԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ��ӦΪAlԪ�أ�Zԭ�ӵ������������Ǵ�����������һ�룬ӦΪSiԪ�أ�X��Zλ��ͬһ���壬��XΪCԪ�أ�Y��Z��Wԭ�ӵ�����������֮��Ϊ14����W������������Ϊ14-3-4=7����ԭ���������ӦΪClԪ�أ�
A��ͬ����Ԫ�ش�����Ԫ�ص�ԭ�Ӱ뾶��С�����Ӳ�Խ��ԭ�Ӱ뾶Խ����ԭ�Ӱ뾶��С�����˳��Ϊ��C��Cl��Si��Al����A����
B��Z�����������Ϊ�������裬�������費����ˮ��Ӧ���ɹ��ᣬ��B����
C��������Al���������������ȷ�Ӧ��������������������C��ȷ��
D�������£�0.1 mol/L HCl��ˮ��Һ��������Դ��HCl��ˮ�ĵ��룬��Һ��������Ũ�Դ���0.1 mol/L����D����
��ѡC��
���� ���⿼��λ�ýṹ���ʹ�ϵӦ�ã��Ѷ��еȣ�ע���Y���ʵ�������Ϊ�ƶ����ͻ�ƿڣ��ѶȲ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | Al3+��NO3-��K+��SO42�� | B�� | Ca2+��H+��CO32����AlO2- | ||
| C�� | OH-��SO42-��NH4+��Ag+ | D�� | Fe2+��Mg2+��H+��NO3�� |
| A�� | ��A��Ԫ����ͬ�����зǽ�������ǿ��Ԫ�� | |
| B�� | ԭ������Ϊ15��Ԫ�ص�����ϼ�Ϊ+3 | |
| C�� | ������������2��Ԫ��һ��λ��Ԫ�����ڱ��ĵڢ�A�� | |
| D�� | �ڶ����ڢ�A��Ԫ�ص�ԭ�Ӻ˵������������һ��Ϊ6 |
| A�� | ǿ������Һ�У�Na+��K+��AlO2-��CO32- | |
| B�� | ���д���Fe3+����Һ�У�NH4+��SCN-��Cl-��K+ | |
| C�� | pH=7����Һ�У�NH4+��Al3+��SO42-��CO32- | |
| D�� | c��OH-��=1��10-13 mol/L����Һ�У�K+��Fe2+��Cl-��NO3- |
��CO��g��+2H2��g��?CH3OH��g����H1=-Q1 kJ•mol-1
��2CH3OH��g��?CH3OCH3��g��+H2O��g����H2=-Q2 kJ•mol-1
��CO��g��+H2O��g��?CO2��g��+H2��g����H3=-Q3 kJ•mol-1
�ش��������⣺
��1���¹��յ��ܷ�Ӧ3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g�����Ȼ�ѧ����ʽΪ3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g����H=-��2Q1+Q2+Q3��kJ/mol��
��2����ҵ��һ���ں����ܱ������в������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH ��g����H���±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
A����ϵ��ѹǿ����
B���ܶȲ���
C������������Է�����������
D��c��CO��=c��CH3OH��
��ij�¶��£��� 2mol CO�� 6mol H2 ����2L���ܱ������У���ַ�Ӧ 10min�ﵽƽ��ʱ���c��CO��=0.2mol/L��������¶��µ�ƽ�ⳣ��K=2.04��
��3����ҵ�����ǰ�ˮú���еĻ�����徭���������õĽϴ�H2���ںϳɰ����ϳɰ���Ӧԭ��Ϊ��N2��g��+3H2��g��$?_{����}^{���¸�ѹ}$ 2NH3��g����H=-92.4kJ•mol-1��ʵ����ģ�⻯���������ں����ܱ������г���һ����N2��H2�ֱ��ڲ�ͬʵ�������·�Ӧ��N2Ũ����ʱ��仯��ͼ1����ش��������⣺
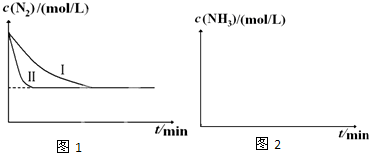
����ʵ���Ƚϣ�ʵ���ı������Ϊ���������
����ʵ����иı�����Ϊ���ñ�ʵ�����ߵ��¶ȣ�����ͼ2�л���ʵ����ʵ�����c��NH3����ʱ��仯��ʾ��ͼ��
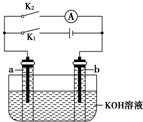 ��ͼ��ʾ��a��b�Ƕ��ʯī�缫��ijͬѧ��ͼʾװ�ý�������ʵ�飺�Ͽ�K2���պ�K1һ��ʱ�䣬�۲쵽��֧�������ڶ������ݽ��缫��Χ����ʱ�Ͽ�K1���պ�K2���۲쵽������A��ָ����ƫת������˵������ȷ���ǣ�������
��ͼ��ʾ��a��b�Ƕ��ʯī�缫��ijͬѧ��ͼʾװ�ý�������ʵ�飺�Ͽ�K2���պ�K1һ��ʱ�䣬�۲쵽��֧�������ڶ������ݽ��缫��Χ����ʱ�Ͽ�K1���պ�K2���۲쵽������A��ָ����ƫת������˵������ȷ���ǣ�������| A�� | �Ͽ�K2���պ�K1һ��ʱ�䣬��Һ��pH��� | |
| B�� | �Ͽ�K1���պ�K2ʱ��b���ϵĵ缫��ӦʽΪ��2H++2e-�TH2�� | |
| C�� | �Ͽ�K2���պ�K1ʱ��a���ϵĵ缫��ӦʽΪ��4OH--4e-�TO2��+2H2O | |
| D�� | �Ͽ�K1���պ�K2ʱ��OH-��b���ƶ� |
 �ܱ�������mA��g��+nB��g��?pC��g������Ӧ�ﵽƽ��״̬�����ⶨ����ѹǿpʱ��A��ת������p���仯��������ͼ��ʾ��
�ܱ�������mA��g��+nB��g��?pC��g������Ӧ�ﵽƽ��״̬�����ⶨ����ѹǿpʱ��A��ת������p���仯��������ͼ��ʾ��