��Ŀ����
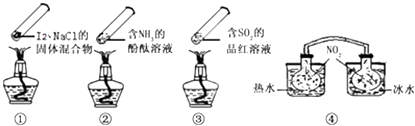
����Ŀ����ͼΪͭ˿��Ũ���ᷴӦ����֤��������ʵ�ʵ��װ�ã�
��1�����з�Ӧ�Ļ�ѧ����ʽ�� �� ����ͭ�����������������ԭ������Ӧ���ж�����Ϊ ��
��2�����б���NaHSO3��Һ�������dz�ȥ���лӷ��������ᣮ����һ��ʱ�������Һ��Ȼ���壬������Һ��ɫ����Ҫ������ֹͭ������ķ�Ӧ����ǡ���ķ����� �� a������ͭ˿��ʹ����������
b����ȥ�ƾ���
c����ȥ������������
��3����Ӧֹͣ��װ����ȴ���Ѣ�ȡ�º�������Һ�ֳ�����������ʵ�飺
�����Լ� | ���� | ��Ӧ�����ӷ���ʽ | |
��һ�� | ����NaOH��Һ | �а�ɫ�������� | |
�ڶ��� | ������ˮ | �а�ɫ�������� |
���������Ӧ�����ӷ���ʽ��
��4���������ŵ������� ��
��5������ʵ��������֢����Թ�����������ɫ������֣���ȴ���Թ��е����ʻ�������ˮ�У���Һ����ɫ��ȡ������ɫ��Һ���Թ��У��μ�NaOH��Һ�����������ֵ������� ��
���𰸡�
��1��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O��������CuԪ�ػ��ϼ�����
CuSO4+SO2��+2H2O��������CuԪ�ػ��ϼ�����
��2��a
��3��SO2+2OH���TSO ![]() +H2O��Ba2++SO
+H2O��Ba2++SO ![]() �TBaSO3����SO2+Cl2+H2O�T4H++2Cl��+SO
�TBaSO3����SO2+Cl2+H2O�T4H++2Cl��+SO ![]() ��Ba2++SO
��Ba2++SO ![]() �TBaSO4��
�TBaSO4��
��4�����ն�������
��5����ʼû��������������ɫ��������
���������⣺��1��ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ�Ͷ�������ˮ����ѧ����ʽ��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O����Ӧ��������ͭ��ͭ�����������Դ��ǣ�Cu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O����Ӧ��������ͭ��ͭ�����������Դ��ǣ�Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O��������CuԪ�ػ��ϼ����ߣ���2�����Ȼӷ����������ܹ����Ȼ�����Ӧ�������ᱵ�������Զ�����������ʼ�����ɸ��ţ����������������Ƴ�ȥ�ӷ������ᣬҪ������ֹͭ������ķ�Ӧ����������ͭ˿��ʹ���������ᣬ��ȥ�ƾ��ƣ���������������ȥ�����������ᣬ�������ӣ����Դ��ǣ�a����3����������Ϊ������������������Ʒ�Ӧ��������������Һ�������������Ȼ�����Ӧ���������ᱵ���������ӷ���ʽ��SO2+2OH���TSO
CuSO4+SO2��+2H2O��������CuԪ�ػ��ϼ����ߣ���2�����Ȼӷ����������ܹ����Ȼ�����Ӧ�������ᱵ�������Զ�����������ʼ�����ɸ��ţ����������������Ƴ�ȥ�ӷ������ᣬҪ������ֹͭ������ķ�Ӧ����������ͭ˿��ʹ���������ᣬ��ȥ�ƾ��ƣ���������������ȥ�����������ᣬ�������ӣ����Դ��ǣ�a����3����������Ϊ������������������Ʒ�Ӧ��������������Һ�������������Ȼ�����Ӧ���������ᱵ���������ӷ���ʽ��SO2+2OH���TSO ![]() +H2O Ba2++SO
+H2O Ba2++SO ![]() �TBaSO3��������������л�ԭ�ԣ��ܹ�����������������������ӣ�������������Ȼ�����Ӧ�������ᱵ���������ӷ���ʽ��SO2+Cl2+H2O�T4H++2Cl��+SO
�TBaSO3��������������л�ԭ�ԣ��ܹ�����������������������ӣ�������������Ȼ�����Ӧ�������ᱵ���������ӷ���ʽ��SO2+Cl2+H2O�T4H++2Cl��+SO ![]() Ba2++SO
Ba2++SO ![]() �TBaSO4�������Դ��ǣ�SO2+2OH���TSO
�TBaSO4�������Դ��ǣ�SO2+2OH���TSO ![]() +H2O��Ba2++SO
+H2O��Ba2++SO ![]() �TBaSO3����SO2+Cl2+H2O�T4H++2Cl��+SO
�TBaSO3����SO2+Cl2+H2O�T4H++2Cl��+SO ![]() ��Ba2++SO
��Ba2++SO ![]() �TBaSO4������4������Ӧ���м�Һ�������ն�������ֹ��Ⱦ���������Դ��ǣ����ն�������5����4����ɫ��Һ�к������������ͭ����������������Һ�����������������ᷴӦ����������ͭ��Ӧ����������Ϊ����ʼû��������������ɫ�������ɣ����Դ��ǣ���ʼû��������������ɫ�������ɣ�
�TBaSO4������4������Ӧ���м�Һ�������ն�������ֹ��Ⱦ���������Դ��ǣ����ն�������5����4����ɫ��Һ�к������������ͭ����������������Һ�����������������ᷴӦ����������ͭ��Ӧ����������Ϊ����ʼû��������������ɫ�������ɣ����Դ��ǣ���ʼû��������������ɫ�������ɣ�