��Ŀ����
����Ŀ��ij��Ӧ�з�Ӧ�����������У�FeCl2��FeCl3��CuCl2��Cu�� 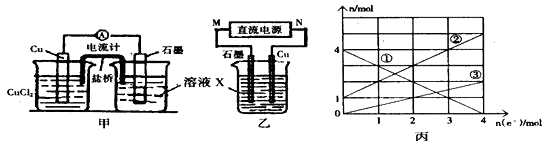
��1����������Ӧ��Ƴɵ�ԭ�����ͼ����ʾ����ش��������⣺ ��ͼ��X��Һ������Cu�缫�Ϸ����ĵ缫��ӦʽΪ��
��ԭ��ع���ʱ�������е����ӣ��K+����Cl���������Ͻ���X��Һ�У�
��2����������Ӧ��Ƴɵĵ�����ͼ����ʾ�����ձ��н��������ӵ����ʵ��������ת�Ƶ����ʵ����ı仯��ϵ��ͼ������ش��������⣺ ��M��������ͼ���еĢ��������ӵı仯��
�۵�����ת��Ϊ2molʱ�������ձ��м���L 5molL��1NaOH��Һ����ʹ���еĽ��������ӳ�����ȫ��
��3��������Ҫ������������ƣ�Na2FeO4����һ����������ˮ�����������кܶ��ŵ㣮 �ٸ���������������֮һ�ǵ�ⷨ����ԭ��ΪFe+2NaOH+2H2O ![]() Na2FeO4+3H2��������ʱ�����ĵ缫��Ӧʽ�� ��
Na2FeO4+3H2��������ʱ�����ĵ缫��Ӧʽ�� ��
�ڸ���������������֮������ǿ���Խ�������NaClO����Fe��OH��3���ɸ������ơ��Ȼ��ƺ�ˮ���÷�Ӧ�����ӷ���ʽΪ ��
��Na2FeO4����������ˮ��ԭ�� ��
���𰸡�
��1��FeCl3��Cu��2e��=Cu2+��K+
��2������Fe2+��2.8
��3��Fe+8OH����6e��=FeO42��+4H2O��2Fe��OH��3+3ClO��+4OH��=2FeO42��+3Cl��+5H2O���������������ԣ���ɱ�����������ɵ�Fe3+ˮ���γɽ��壬��������������ľ�ˮ����
���������⣺��1���پݷ�Ӧ������������ȷ�����з�ӦΪ2FeCl3+Cu�T2FeCl2+CuCl2 �� ��XΪFeCl3 �� ���Դ��ǣ�FeCl3�� ��ͭ������ʧ���ӷ���������Ӧ���缫��ӦΪCu��2e��=Cu2+ �� ���Դ��ǣ�Cu��2e��=Cu2+����Cu��������ʯī���������������������������ƶ�����K+������������������X��Һ�У����Դ��ǣ�K+�� ��2���ٸ��ݱ�ͼ��֪��Һ�������ֽ��������ӣ�������X�ijɷֿ�֪X��ֻ�����ֽ��������ӣ�˵���ڵ������л���Cu2+���ɣ����Cu��������ʯī����������MΪ������NΪ���������Դ��ǣ��������ڵ���������Cu2+���ɣ���Cu2+�����ʵ����������������Ԣ�ΪCu2+ �� ��ͼ��֪���ٱ�ʾ�Ľ������ӵ����ʵ����������٣���ΪFe3+ �� ���Ԣ�ΪFe2+ �� ���Դ��ǣ�Fe2+�� �۵�����ת��Ϊ2molʱ����Һ����Fe3+ 2mol��Fe2+ 3mol��Cu2+Ϊ1mol��������Ҫ����NaOH��Һ14mol������NaOH��Һ�����Ϊ ![]() =2.8L�����Դ��ǣ�2.8����3��������������������������Ʊ������ƣ����ʱ��ʧȥ���ӷ���������Ӧ�������������������������Ӻ�ˮ���缫��ӦʽΪ��Fe+8OH����6e��=FeO42��+4H2O�����Դ��ǣ�Fe+8OH����6e��=FeO42��+4H2O����NaClO����Fe��OH��3�ķ�Ӧ����ʽΪ2Fe��OH��3+3ClO��+4OH���T2FeO42��+3Cl��+5H2O�����Դ��ǣ�2Fe��OH��3+3ClO��+4OH���T2FeO42��+3Cl��+5H2O����Na2FeO4����������ˮ��ԭ���Ǹ������������ԣ�������ɱ��������Fe3+�γɽ��壬��������������ľ�ˮ�����ã����Դ��ǣ��������������ԣ���ɱ�����������ɵ�Fe3+ˮ���γɽ��壬��������������ľ�ˮ���ã�
=2.8L�����Դ��ǣ�2.8����3��������������������������Ʊ������ƣ����ʱ��ʧȥ���ӷ���������Ӧ�������������������������Ӻ�ˮ���缫��ӦʽΪ��Fe+8OH����6e��=FeO42��+4H2O�����Դ��ǣ�Fe+8OH����6e��=FeO42��+4H2O����NaClO����Fe��OH��3�ķ�Ӧ����ʽΪ2Fe��OH��3+3ClO��+4OH���T2FeO42��+3Cl��+5H2O�����Դ��ǣ�2Fe��OH��3+3ClO��+4OH���T2FeO42��+3Cl��+5H2O����Na2FeO4����������ˮ��ԭ���Ǹ������������ԣ�������ɱ��������Fe3+�γɽ��壬��������������ľ�ˮ�����ã����Դ��ǣ��������������ԣ���ɱ�����������ɵ�Fe3+ˮ���γɽ��壬��������������ľ�ˮ���ã�

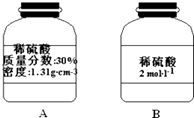
����Ŀ����ͼΪͭ˿��Ũ���ᷴӦ����֤��������ʵ�ʵ��װ�ã�
��1�����з�Ӧ�Ļ�ѧ����ʽ�� �� ����ͭ�����������������ԭ������Ӧ���ж�����Ϊ ��
��2�����б���NaHSO3��Һ�������dz�ȥ���лӷ��������ᣮ����һ��ʱ�������Һ��Ȼ���壬������Һ��ɫ����Ҫ������ֹͭ������ķ�Ӧ����ǡ���ķ����� �� a������ͭ˿��ʹ����������
b����ȥ�ƾ���
c����ȥ������������
��3����Ӧֹͣ��װ����ȴ���Ѣ�ȡ�º�������Һ�ֳ�����������ʵ�飺
�����Լ� | ���� | ��Ӧ�����ӷ���ʽ | |
��һ�� | ����NaOH��Һ | �а�ɫ�������� | |
�ڶ��� | ������ˮ | �а�ɫ�������� |
���������Ӧ�����ӷ���ʽ��
��4���������ŵ������� ��
��5������ʵ��������֢����Թ�����������ɫ������֣���ȴ���Թ��е����ʻ�������ˮ�У���Һ����ɫ��ȡ������ɫ��Һ���Թ��У��μ�NaOH��Һ�����������ֵ������� ��