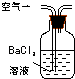题目内容
【题目】要增大铁与盐酸反应的速率,所采取的下列措施中无效的是( )
A.用铁粉代替铁片
B.增大压强
C.提高反应的温度
D.增大盐酸的浓度
【答案】B
【解析】解:A.用铁粉代替铁片,增大了反应物的接触面积,反应速率加快,故A不选;B.该反应为溶液中的反应,受压强影响不大,则增大压强,不能增大Fe与盐酸的反应速率,故B选;
C.提高反应的温度,反应的速率加快,故C不选;
D.增大盐酸的浓度,氢离子浓度变大,反应速率加快,故D不选.
故选B.
增大铁与盐酸反应的速率,则增大接触面积、酸的浓度、温度等,该反应为溶液中的反应,受压强影响不大,以此来解答.

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案【题目】恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g).反应过程中测定的部分数据如表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2)/mol |
0 | 2.0 | 2.0 | 0 |
2 | 0.8 | ||
4 | 1.2 | ||
6 | 1.2 | 2.8 |
下列说法正确的是( )
A.0~2 min内的平均速率为υ (CO)=0.6 mol/(Lmin)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)=0.6 mol
【题目】填空题
(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是(填序号)
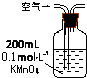
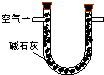
序号 | A | B | C |
装置 |
|
|
|
原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g.由此推知气体Y中SO2的体积分数为 .