题目内容
【题目】生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12 000~20 000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 | N≡N | F-F | N-F |
键能/kJ·mol-1 | 941.7 | 154.8 | 283.0 |
下列说法中正确的是
A.过程N2(g)![]() 2N(g)放出能量
2N(g)放出能量
B.过程N(g)+3F(g)![]() NF3(g)放出能量
NF3(g)放出能量
C.反应N2(g)+3F2(g)![]() 2NF3(g)吸收热量
2NF3(g)吸收热量
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
【答案】B
【解析】由N2(g)→2N(g)为化学键的断裂过程,应吸收能量,A项错误;由N(g)+3F(g)→NF3(g)为形成化学键的过程,放出能量,B项正确;反应N2(g)+3F2(g)=2NF3(g) ΔH=(941.7+3×154.8-283.0×6)kJ·mol1= 291.9 kJ·mol-1,ΔH<0,放出热量,C项错误;NF3吸收能量后如果没有化学键的断裂与生成,则不能发生化学反应,化学反应的实质是旧键的断裂和新键的形成,D项错误。

【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:; 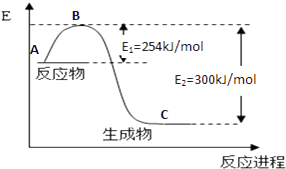
(2)若已知下列数据:
化学键 | H﹣H | N≡N |
键能/kJmol﹣1 | 435 | 943 |
试根据表中及图中数据计算N﹣H的键能kJmol﹣1
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1和E2的变化是:E1 , E2(填“增大”、“减小、”“不变”).
(4)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
若1mol NH3还原NO至N2 , 则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)