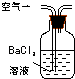题目内容
【题目】填空题
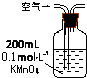
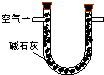
(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是(填序号)
序号 | A | B | C |
装置 |
|
|
|
原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g.由此推知气体Y中SO2的体积分数为 .
【答案】
(1)BC
(2)66.7%
【解析】解:(1.)A、二氧化硫与氯化钡不能反应,故A不能测出空气中SO2含量,该方法不可行;B、二氧化硫能被高锰酸钾氧化生成硫酸,所以根据高锰酸钾溶液的质量的增加可知二氧化硫的质量,该方法可行;C、二氧化硫能与氢氧化钠反应生成亚硫酸钠,根据氢氧化钠溶液的质量的增加可知二氧化硫的质量,该方法可行;所以答案是:AB;
(2.)SO2和溴水反应生成硫酸和氢溴酸,加入足量BaCl2溶液,生成硫酸钡2.33g即0.01mol,根据硫元素守恒可知SO2的物质的量为0.01mol,SO2的体积分数为 ![]() ×100%=66.7%,所以答案是:66.7%;
×100%=66.7%,所以答案是:66.7%;

练习册系列答案
相关题目