��Ŀ����
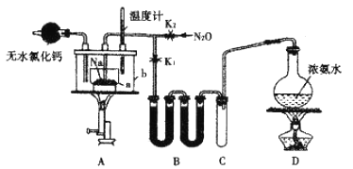
����Ŀ����������(NaN3)��һ��������ˮ�İ�ɫ���壬�����Ҵ������������ѣ������ںϳɿ�����ͷ�߾���ҩ����м��塢������ȫ���ҵ�ҩ���ȡ�������(NaNH2)���۵�Ϊ210�棬�е�Ϊ400�棬��ˮ��Һ����ˮ�⡣ʵ������ȡ�������Ƶ�ʵ�鲽�輰ʵ��װ�����£�
�ٴ�ֹˮ��K1���ر�ֹˮ��K2������װ��Dһ��ʱ�䣻
�ڼ���װ��A�еĽ����ƣ�ʹ���ۻ�����ַ�Ӧ����ֹͣ����װ��D���ر�K1��
����װ��A��b�����ڼ�����Ƚ��ʲ����ȵ�210��220�棬��ֹˮ��K2��ͨ��N2O��
����ȴ��������м����Ҵ�����ѹŨ���ᾧ���ٹ��ˣ���������ϴ�ӣ����ɡ�
�ش��������⣺
(1)װ��B��ʢ�ŵ�ҩƷΪ____________��
(2)�������ۻ����Ʒ�Ӧ����NaNH2�Ļ�ѧ����ʽΪ__________��
(3)������У�Ϊ��ʹ��Ӧ���Ⱦ��ȣ�Aװ����a�����ļ��ȷ�ʽΪ__________������NaN3�Ļ�ѧ����ʽΪ__________��N2O����NH4NO3��240~245��ֽ��Ƶ�(����淋��۵�Ϊ169.6��)����Ӧѡ������巢��װ����_____________(�����)��

(4)�������������ϴ�ӵ���ҪĿ����______________��
(5)ʵ�����õζ����ⶨ����������Ʒ��NaN3������������
�ٽ�2.500g�������500.00mL��Һ��
��ȡ50.00mL��Һ������ƿ�У�����50.00mL0.1010mol/L(NH4)2Ce(NO3)6��Һ��
�۳�ַ�Ӧ����Һ��ϡ�ͣ�����Һ�м���8mLŨ���ᣬ����3���ڷƆ���ָʾҺ����0.0500mol/L(NH4)2Fe(SO4)2����Һ�ζ�������Ce4+������Һ���Ϊ29.00mL���ⶨ���̵ķ�Ӧ����ʽΪ��2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2����Ce4++Fe2+=Ce3++Fe3+����������NaN3����������Ϊ_______________��
���𰸡���ʯ��(���������ƹ���) 2Na+2NH3![]() 2NaNH2+H2 ��ԡ NaNH2+N2O
2NaNH2+H2 ��ԡ NaNH2+N2O![]() NaN3+H2O ��� NaN3���������ѣ��ܼ���NaN3���ܽ���ģ��������ӷ��������ڲ�Ʒ���ٸ��� 93.60%
NaN3+H2O ��� NaN3���������ѣ��ܼ���NaN3���ܽ���ģ��������ӷ��������ڲ�Ʒ���ٸ��� 93.60%
��������
(1)NaN3��������ˮ�����Ʊ����̲�����ˮ�IJ��룻
(2)�������ۻ����Ʒ�Ӧ����NaNH2��������
(3)����۵��¶�Ϊ210��220�棬ѡ����ԡ���ȣ�NaNH2��N2O��̬���еõ�NaN3����������淋��۵�Ϊ169.6�棬��NH4NO3��240��245��ֽ⣬��ѡ������Ӧ����������ۻ�����ֹ�����Թܵײ���
(4) NaN3��������ˮ�İ�ɫ���壬�����Ҵ�������������,���������ӷ�������
(5)(NH4)2Ce(NO3)6���ܵ����ʵ���Ϊ��0.1010mol/L��50��10-3L=0.00505mol��������������Ʒ�Ӧ��ʣ���(NH4)2Ce(NO3)6��(NH4)2Fe(SO4)2����Һ�ζ���������֪��Ӧ��Ce4++Fe2+=Ce3++Fe3+�����뷴Ӧ��(NH4)2Ce(NO3)6���Һ�����ʵ�����ȣ�Ϊ��0.0500mol/L��29.00��10-3L=0.00145mol������������Ʒ�Ӧ��(NH4)2Ce(NO3)6�����ʵ���Ϊn[(NH4)2Ce(NO3)6]=0.00505mol-0.00145mol=0.0036mol�����ݷ�Ӧ�У�NaN3��(NH4)2Ce(NO3)6����2.500g�����е������Ƶ�����Ϊ0.0036mol��65g/mol��![]() =2.34g���Դ������
=2.34g���Դ������
(1)��NaN3������ˮ��������Ʊ����̲�����ˮ����װ��Bʢ�е��Լ��Ǽ�ʯ�ң����������ƹ��壩��
(2)�������ۻ����Ʒ�Ӧ����NaNH2����������ӦΪ��2Na+2NH3![]() 2NaNH2+H2��
2NaNH2+H2��
(3)����۵��¶�Ϊ210��220�棬��ѡ��ļ��ȷ�ʽΪ��ԡ���ȣ�NaNH2+N2O![]() NaN3+H2O������淋��۵�Ϊ169.6�棬��NH4NO3��240��245��ֽ⣬Ϊ��ֹ������ۻ������Թܵײ�����ѡ������巢��װ����I��III������ѡII��
NaN3+H2O������淋��۵�Ϊ169.6�棬��NH4NO3��240��245��ֽ⣬Ϊ��ֹ������ۻ������Թܵײ�����ѡ������巢��װ����I��III������ѡII��
(4)�����֪��NaN3���������ѣ��ܼ���NaN3���ܽ���ģ��������ӷ��������ڲ�Ʒ���ٸ���ʲ������������ϴ�ӵ���ҪĿ���dz�ȥ�Ҵ�������NaN3���ܽ���ģ������ڲ�Ʒ���ٸ��
(5) (NH4)2Ce(NO3)6���ܵ����ʵ���Ϊ��0.1010mol/L��50��10-3L=0.00505mol��������������Ʒ�Ӧ��ʣ���(NH4)2Ce(NO3)6��(NH4)2Fe(SO4)2����Һ�ζ���������֪��Ӧ��Ce4++Fe2+=Ce3++Fe3+�����뷴Ӧ��(NH4)2Ce(NO3)6���Һ�����ʵ�����ȣ�Ϊ��0.0500mol/L��29.00��10-3L=0.00145mol������������Ʒ�Ӧ��(NH4)2Ce(NO3)6�����ʵ���Ϊn[(NH4)2Ce(NO3)6]=0.00505mol-0.00145mol=0.0036mol�����ݷ�Ӧ�У�NaN3��(NH4)2Ce(NO3)6����2.500g�����е������Ƶ�����Ϊ0.0036mol��65g/mol��![]() =2.34g����������NaN3����������Ϊ
=2.34g����������NaN3����������Ϊ![]() ��100%=93.60%��
��100%=93.60%��

 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д�