题目内容
用铂电极电解CuSO4溶液,当[Cu2+]调低至原来的一半时停止通电,若加入下面物质能使溶液恢复成原来浓度的是
| A.无水CuSO4 |
| B.CuO |
| C.Cu(OH)2 |
| D.CuSO4·5H2O |
B
用铂电极电解CuSO4时,反应的总方程式为:
2CuSO4+2H2O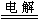 2Cu↓+2H2SO4+O2↑
2Cu↓+2H2SO4+O2↑
当[Cu2+]降为原来的一半时,消耗了一半的Cu2+,同时又放出一定量的O2使电解液中的H2O也减小一半的量,要恢复原浓度,既需补充Cu2+,又需补充H2O,而且要使生成的H2SO4完全变成SO42-,H+复原为H2O。只能用碱性氧化物或碱。又由于:CuO+H2SO4====CuSO4+H2OCu(OH)2+H2SO4====CuSO4+2H2O,按电解方程式:CuSO4~H2O~H2SO4,所以应选CuO,若用Cu(OH)2,会增加H2O量,使[Cu2+]小于原来的浓度值。
2CuSO4+2H2O
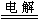 2Cu↓+2H2SO4+O2↑
2Cu↓+2H2SO4+O2↑当[Cu2+]降为原来的一半时,消耗了一半的Cu2+,同时又放出一定量的O2使电解液中的H2O也减小一半的量,要恢复原浓度,既需补充Cu2+,又需补充H2O,而且要使生成的H2SO4完全变成SO42-,H+复原为H2O。只能用碱性氧化物或碱。又由于:CuO+H2SO4====CuSO4+H2OCu(OH)2+H2SO4====CuSO4+2H2O,按电解方程式:CuSO4~H2O~H2SO4,所以应选CuO,若用Cu(OH)2,会增加H2O量,使[Cu2+]小于原来的浓度值。

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
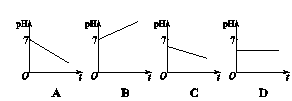
 KIO3+3H2↑。
KIO3+3H2↑。