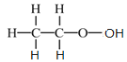
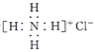题目内容
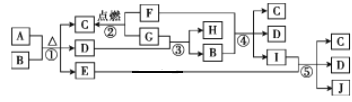
【题目】有关物质的转化关系如图所示。C为常见的调味品,D是常见的无色液体。E、F、H和J均为气体,其中H和J为单质,且两者在一定条件下可生成E。
(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有__性。
(2)写出反应①的化学方程式:_____。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目:___。
(4)写出反应④的离子方程式:____。
(5)写出反应⑤的化学方程式:____。
【答案】(强)氧化 NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O ![]() Cl2+2OH-
Cl2+2OH-![]() Cl-+ClO-+H2O 2NH3+3NaClO
Cl-+ClO-+H2O 2NH3+3NaClO![]() 3NaCl+N2↑+3H2O
3NaCl+N2↑+3H2O
【解析】
C为常见的调味品,则C为NaCl;F和G在点燃条件下反应生成NaCl,F为气体,则F为Cl2,G为Na;其中D是常见的无色液体,则D为H2O;Na和H2O反应生成NaOH和H2(H和B),H为气体单质,则H为H2,B为NaOH,Cl2和NaOH反应生成NaCl、NaClO和H2O(C、D和I),则I为NaClO,A和B(NaOH)反应能生成E,E为气体,则E为NH3,A为NH4Cl,H和J为单质且两者在一定条件下可生成E,则J为N2,则NH3和NaClO反应生成NaCl、N2和H2O,据此答题。
(1)物质I为NaClO,其溶液可用作家用消毒剂、漂白液,是因为具有强氧化性,故答案为:(强)氧化。
(2)反应①为NH4Cl与NaOH在加热条件下反应生成NaCl、NH3和H2O,化学方程式为:NH4Cl+NaOH![]() NaCl+NH3↑+H2O,故答案为:NH4Cl+NaOH
NaCl+NH3↑+H2O,故答案为:NH4Cl+NaOH![]() NaCl+NH3↑+H2O。
NaCl+NH3↑+H2O。
(3)反应③为Na和H2O反应生成NaOH和H2,化学方程式为:2Na +2H2O=2NaOH +H2↑,该反应中钠的化合价由0价升高为+1价,H元素的化合价由+1价降低为0价,转移2个电子,用单线桥表示电子转移的方向和数目为:![]() ,故答案为:
,故答案为:![]() 。
。
(4)反应④为Cl2和NaOH反应生成NaCl、NaClO和H2O,离子方程式为:Cl2+2OH-![]() Cl-+ClO-+H2O,故答案为:Cl2+2OH-
Cl-+ClO-+H2O,故答案为:Cl2+2OH-![]() Cl-+ClO-+H2O。
Cl-+ClO-+H2O。
(5)反应⑤为NH3和NaClO反应生成NaCl、N2和H2O,化学方程式2NH3+3NaClO![]() 3NaCl+N2↑+3H2O,故答案为:2NH3+3NaClO
3NaCl+N2↑+3H2O,故答案为:2NH3+3NaClO![]() 3NaCl+N2↑+3H2O。
3NaCl+N2↑+3H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案