题目内容
14.下列电子式书写正确的是( )| A. | NaCl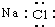 | B. | OH-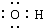 | C. | HCl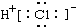 | D. | Na2O2 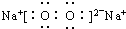 |
分析 A.氯化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
B.OH-为带1个负电荷的阴离子,需要标出离子中各原子最外层电子;
C.氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子;
D.过氧化钠是离子化合物.
解答 解:A.氯化钠属于离子化合物,电子式中钠离子形成离子符号形式,氯离子需要标出最外层电子,氯化钠正确的电子式为 ,故A错误;
,故A错误;
B.氢氧根离子为带有1个单位负电荷的阴离子,需要标出离子中各原子最外层电子,氢氧根离子的电子式为: ,故B错误;
,故B错误;
C.氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为 ,故C错误;
,故C错误;
D.过氧化钠由钠离子与过氧根离子过程,电子式为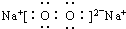 ,故D正确.故选D.
,故D正确.故选D.
点评 本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
相关题目
4.某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原HNO3的物质的量之比为2:1时,还原产物可能是( )
| A. | N2O | B. | NO | C. | NO2 | D. | N2 |
2.下列说法正确的是( )
| A. | 决定有机物种类繁多的原因是组成有机物的元素种类较多 | |
| B. | C5H12有四种同分异构体 | |
| C. |  用系统命名法命名:3,4,4-三甲基-6-乙基庚烷 用系统命名法命名:3,4,4-三甲基-6-乙基庚烷 | |
| D. |  与 与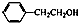 互为同系物 互为同系物 |
9.下列说法正确的是( )
| A. | 室温下,将pH=2的醋酸与pH=12的NaOH溶液等体积混合,溶液显中性 | |
| B. | 室温下,向pH=3的醋酸溶液加水稀释后,溶液中所有离子浓度均减小 | |
| C. | 向含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| D. | 为保护地下钢管不受腐蚀,可将它与直流电源的负极相连 |
19.下列说法不正确的是( )
| A. | CS2 与CO2均为直线形非极性分子 | |
| B. | 熔点:SiCl4<MgCl2<SiO2 | |
| C. | 水加热到很高的温度都难以分解,是因为水中含有氢键 | |
| D. | 断裂化学键的过程不一定发生化学变化 |
6.下列有关物质的用途错误的是( )
| A. | 水玻璃可用作木材防火剂 | B. | 二氧化硅是制造光导纤维的材料 | ||
| C. | 可用氢氟酸刻蚀玻璃 | D. | 石英是制造太阳能电池的常用材料 |
3.化学家借助太阳能产生的电能和热能,用空气和水作原料合成了氨气.下列有关说法正确的是( )
| A. | 该合成中所有的电能和热能全部转化为化学能 | |
| B. | 该合成氨过程不属于氮的固定 | |
| C. | 空气、水、太阳能均为可再生资源 | |
| D. | 断裂N2中的N≡N键会释放出能量 |
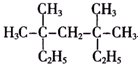 3,3,5,5-四甲基庚烷.
3,3,5,5-四甲基庚烷. .
. .
.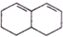 与Br2发生1,4-加成反应的化学方程式为
与Br2发生1,4-加成反应的化学方程式为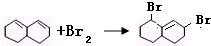 .
.