题目内容
【题目】甲醇![]() 是重要的溶剂和替代燃料,工业上用CO和
是重要的溶剂和替代燃料,工业上用CO和![]() 在一定条件下制备
在一定条件下制备![]() 的反应为:
的反应为:![]() ,在体积为1L的恒容密闭容器中,充人
,在体积为1L的恒容密闭容器中,充人![]() 和
和![]() ,一定条件下发生上述反应,测得
,一定条件下发生上述反应,测得![]() 和
和![]() 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:

![]() 从反应开始至达到平衡,用氢气表示的平均反应速率
从反应开始至达到平衡,用氢气表示的平均反应速率![]() ______
______![]()
![]() 下列说法正确的是______
下列说法正确的是______![]() 填字母序号
填字母序号![]() 。
。
A.达到平衡时,CO的转化率为![]()
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前![]() 正
正![]() 逆
逆![]() ,2min后
,2min后![]() 正
正![]() 逆
逆![]()
![]() 该条件下反应的平衡常数
该条件下反应的平衡常数![]() ______。
______。
【答案】![]() AB 3
AB 3
【解析】
![]() 从反应开始到5min,CO的物质的量浓度改变量为
从反应开始到5min,CO的物质的量浓度改变量为![]() ,根据
,根据![]() 先计算CO的反应速率,再根据化学反应速率与化学计量数成正比计算
先计算CO的反应速率,再根据化学反应速率与化学计量数成正比计算![]() ;
;
![]() 达到平衡时,CO的物质的量浓度改变量为
达到平衡时,CO的物质的量浓度改变量为![]() ,转化率等于转化量与总量的比值;
,转化率等于转化量与总量的比值;
B. 混合气体的平均相对分子质量大小为![]() ,反应前后质量守恒,m不变,总物质的量随着反应进行发生改变,5min时反应到达化学平衡,n不变,则混合气体的平均相对分子质量不再改变;
,反应前后质量守恒,m不变,总物质的量随着反应进行发生改变,5min时反应到达化学平衡,n不变,则混合气体的平均相对分子质量不再改变;
C. 达到平衡后,恒温恒容,充入无关气体,反应速率不变;
D. 2min时反应尚未达到平衡,反应仍需正向进行,5min反应才达到平衡,平衡前始终满足![]() ;
;
③根据已知信息可列出三段式,计算出平衡时刻各物质的浓度即可列式计算该温度下该反应的平衡常数。
![]() 从反应开始到5min,CO的物质的量浓度改变量为
从反应开始到5min,CO的物质的量浓度改变量为![]() ,则CO的消耗速率为
,则CO的消耗速率为![]() ,化学反应速率与化学计量数成正比,则
,化学反应速率与化学计量数成正比,则![]() ;
;
故答案为:![]() ;
;
![]() 达到平衡时,CO的物质的量浓度改变量为
达到平衡时,CO的物质的量浓度改变量为![]() ,CO的初始浓度为:
,CO的初始浓度为:![]() ,则CO的转化率为:
,则CO的转化率为:![]() ,故A正确;
,故A正确;
B. 混合气体的平均相对分子质量大小为![]() ,反应前后质量守恒,m不变,总物质的量改变,当反应到达化学平衡时,n不变,则5min后容器中混合气体的平均相对分子质量不再改变,故B正确;
,反应前后质量守恒,m不变,总物质的量改变,当反应到达化学平衡时,n不变,则5min后容器中混合气体的平均相对分子质量不再改变,故B正确;
C. 达到平衡后,再充入氩气,反应为恒容装置,不改变各组分的浓度,所以反应速率不变,故C错误;
D. 2min时反应尚未达到平衡,反应仍需正向进行,所以2min前及![]() 前始终满足
前始终满足![]() ,故D错误;
,故D错误;
故答案为:AB;
③根据已知信息可列出三段式,
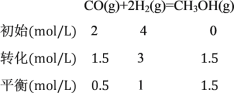 ,则该温度下该反应的平衡常数
,则该温度下该反应的平衡常数![]() ;
;
故答案为:3。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案