题目内容
14.下列说法中,正确的是( )| A. | 放热反应的发生均无需加热 | |
| B. | 需要加热后才能发生的反应均是吸热反应 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 物质发生化学反应都伴随着能量变化 |
分析 A.反应放热还是吸热与反应条件无关,决定于反应物与生成物的能量差;
B.反应放热还是吸热与反应条件无关,决定于反应物与生成物的能量差;
C.物质的三态变化有能量变化,是物理变化;
D.化学变化是旧键断裂新键形成的过程,断键成键都有能量变化.
解答 解:A.燃烧都是放热的但需加热到着火点,故A错误;
B.燃烧都是放热的但需加热到着火点,故B错误;
C.物质的三态变化有能量变化,是物理变化,故C错误;
D.化学变化是旧键断裂新键形成的过程,断键成键都有能量变化,故D正确.
故选:D.
点评 本题考查反应热与反应条件无关,只决定于反应物和生成物的能量高低,同时考查了化学反应中能量变化的原因.

练习册系列答案
相关题目
4.宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”的原理是4Ag+2H2S+O2═2Ag2S+2H2O,下列说法正确的是( )
| A. | Ag是还原剂 | B. | 银针验毒时,空气中氧气失去电子 | ||
| C. | 反应中Ag和H2S均是还原剂 | D. | Ag2S既是氧化产物又是还原产物 |
5.对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是( )
| A. | v(B2)=0.8 mol/(L•s) | B. | v(A2)=0.4 mol/(L•s) | C. | v(C)=0.6 mol/(L•s) | D. | v(B2)=1.0 mol/(L•s) |
2.下表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
(1)F元素在周期表中的位置是第三周期第ⅢA族.
(2)写出C元素氢化物的电子式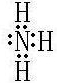 .
.
(3)C和D两种元素氢化物的稳定性更强的是H2O>NH3(填物质的化学式)
(4)用电子式表示离子化合物EG的形成过程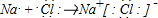 .
.
| A | |||||||
| B | C | D | |||||
| E | F | G | |||||
(2)写出C元素氢化物的电子式
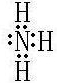 .
.(3)C和D两种元素氢化物的稳定性更强的是H2O>NH3(填物质的化学式)
(4)用电子式表示离子化合物EG的形成过程
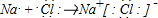 .
.
9.已知同周期X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断正确的是( )
| A. | 在三种元素中,元素Z的非金属性最强 | |
| B. | 气态氢化物的还原性按X、Y、Z的顺序逐渐增强 | |
| C. | Y元素一定是硫 |
19.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(Y)>r(Z)>r(W) | |
| B. | 元素Z、W的简单离子的电子层结构不同 | |
| C. | 元素Y的简单气态氢化物的热稳定性比Z的强 | |
| D. | 只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
6.用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,不需要使用的玻璃仪器是( )
| A. | 圆底烧瓶 | B. | 玻璃棒 | C. | 容量瓶 | D. | 胶头滴管 |
3.下列表示对应化学反应的离子方程式正确的是( )
| A. | 工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- | |
| B. | 碳酸钠的水解:CO32-+2H2O═H2CO3+2OH- | |
| C. | 硫酸铝溶液中滴加过量浓氨水:Al3++4 NH3•H2O═AlO${\;}_{2}^{-}$+4NH4++2H2O | |
| D. | 用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
5.下列装置能组成原电池产生电流的是( )
| A. |  | B. |  | C. |  | D. |  |