题目内容
【题目】(1)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
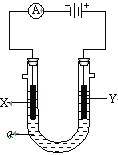
①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中X极现象为__________________________,电极反应式为___________________ 。
②如要用电解方法精炼粗铜,电解液a选用_________溶液,则Y电极的材料是________ 。
③如要在铁上镀银,电解液选用硝酸银,则X电极的材料是_________,电极反应式是_________________。
(2)下图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:2Fe+2H2O+O2=2Fe(OH)2。Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈。请根据图示,回答下列问题:

在上述电化学腐蚀中,碳(C)作_______极,写出负极的电极反应式_________________。如果将长期浸泡在河水中的钢铁闸门与外加电源连接防腐,应将闸门连接外部直流电源的_______极。
【答案】 产生无色气泡 ,溶液变红色 2 H++2e—=H2↑ CuSO4(可溶性铜盐溶液) 粗铜 铁 Ag+ + e—=Ag 正 Fe-2e-= Fe2+ 负
【解析】(1). ①. 若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,由装置图可知,X极连接外加电源的负极,则X为阴极,电极反应式为:2H++2e-= H2↑,X极有无色气泡产生,X极附近溶液碱性增强,溶液变红色,故答案为:产生无色气泡 ,溶液变红色;2H++2e-= H2↑;
②. 如要用电解方法精炼粗铜,电解液a应选用CuSO4(可溶性铜盐溶液),Y为阳极,则Y电极材料为粗铜,故答案为:CuSO4(可溶性铜盐溶液);粗铜;
③. 如要在铁上镀银,电解液选用硝酸银溶液,待镀金属作阴极,镀层金属作阳极,因X电极为阴极,则X电极的材料是铁,银离子在阴极得电子生成单质银,电极反应式为Ag+ + e-=Ag,故答案为:铁;Ag+ + e-=Ag;
(2). 据图可知,钢铁在潮湿空气中发生电化学腐蚀时,氧气在碳电极得电子发生还原反应,则碳为正极,在负极上,铁失电子生成亚铁离子,电极反应式为Fe-2e-= Fe2+,金属在电解池中作阴极时受保护,如果将长期浸泡在河水中的钢铁闸门与外加电源连接防腐,应将闸门连接直流电源的负极,故答案为:正;Fe-2e-= Fe2+;负。

 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案