题目内容
4.25℃时,已知弱酸的电离常数:K(CH3COOH)=1.8×10-5;K1(H2CO3)=4.4×10-7;K2(H2CO3)=4.7×10-11;K(HClO)=4.0×10-8.则下列说法正确的是( )| A. | 新制氯水与碳酸氢钠不反应 | |
| B. | 25℃时,0.1mol/L的醋酸溶液与0.01mol/L的醋酸溶液中,Ka前者小于后者 | |
| C. | NaClO溶液中通入少量二氧化碳的反应为:2NaClO+CO2+H2O=Na2CO3+2HClO | |
| D. | 等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH pH(Na2CO3)>pH(NaClO)>pH(CH3COONa) |
分析 弱酸的电离常数越大,其电离程度越大,则酸性越强,则酸根离子的水解程度越小,结合强酸制取弱酸分析解答,注意水解是微弱的、酸的电离常数只与温度有关.
解答 解:弱酸的电离常数越大,其电离程度越大,则酸性越强,则酸根离子的水解程度越小,根据电离平衡常数知,酸性强弱顺序是:CH3COOH>H2CO3>HClO>HCO3-,
A、新制氯水中含有盐酸和次氯酸,盐酸和碳酸氢钠反应,故A错误;
B、温度相同,则醋酸的电离常数相同,故B错误;
C、酸性强弱顺序是:CH3COOH>H2CO3>HClO>HCO3-,向NaClO溶液中通少量CO2:CO2+NaClO+H2O→NaHCO3+HClO,而不是生成Na2CO3,故C错误;
D、等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液中,pH大小顺序是pH[Na2CO3(aq)]>pH[NaClO(aq)]>pH[CH3COONa(aq)],故D正确;
故选D.
点评 本题考查了弱电解质的电离,明确酸性强弱与其电离程度、酸根离子水解程度的关系是解本题关键,难度中等.

练习册系列答案
相关题目
10.常温离子液体也称常温熔融盐,硝酸乙基铵[(C2H5NH3)NO3]是人类发现的第一种常温离子液体,其熔点为12℃.已知C2H5NH2的化学性质与NH3相似,C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是( )
| A. | 硝酸乙基铵水溶液呈碱性 | |
| B. | 该离子液体可以作为电池的电解质 | |
| C. | (C2H5NH3)NO3能与氢氧化钠反应产生NH3 | |
| D. | 相同温度下,相同物质的量的浓度的硝酸乙基铵溶液和硝酸铵溶液相比前者的pH小 |
9.下列离子方程式中不正确的是( )
| A. | 将盐酸加入稀氨水中 H++NH3•H2O═NH4++H2O | |
| B. | 以酚酞为指示剂用标准盐酸滴定苏打溶液CO32-+2H+═CO2↑+H2O | |
| C. | 氯化铝溶液与氢氧化钠溶液混合后,铝元素有一半转化为偏铝酸钠2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| D. | 用氯气与石灰浆生产漂白粉 Ca(OH)2+Cl2═Ca2++Cl-+ClO-+H2O |
16.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 某物质的结构为 ,与其互为同分异构且完全水解后产物相同的油脂有两种 ,与其互为同分异构且完全水解后产物相同的油脂有两种 | |
| C. | 用溴水即可鉴别四氯化碳、2-己烯和甲苯 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
13. 已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )
 已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )| A. | 原AgNO3溶液的物质的量浓度为0.1 mol•L-1 | |
| B. | 图中X点的坐标为(10,6) | |
| C. | 图中X点对应溶液中Ag+与Cl-的浓度不相同 | |
| D. | 若把0.1 mol•L-1的NaCl溶液换成0.1 mol•L-1的NaI溶液,则图象在终点后变为虚线部分 |
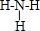 ,D2C含有的化学键类型为离子键;
,D2C含有的化学键类型为离子键; ;
; ;
;