题目内容
13.通常情况下加入氧化剂能实现的变化是( )| A. | MnO2→MnSO4 | B. | Na2O2→O2 | C. | KI→KIO3 | D. | AlCl3→Al(OH)3 |
分析 需要加入氧化剂才能实现,说明选项中物质作还原剂,在反应中失电子化合价升高,据此分析解答.
解答 解:A.该反应中Mn元素化合价由+4价变为+2价,则二氧化锰得电子作氧化剂,需要还原剂才能实现,故A错误;
B.该反应中O元素化合价由-1价变为0价,不需要加入氧化剂就能实现,如过氧化钠和水或二氧化碳反应生成氧气,故B错误;
C.该反应中I元素化合价由-1价变为+5价,失电子作还原剂,需要氧化剂才能实现,故C正确;
D.该反应中Al元素化合价不变,不需要发生氧化还原反应就能实现,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考查,侧重考查学生分析判断能力,熟悉常见元素化合价即可解答,易错选项是B,注意过氧化钠的性质.

练习册系列答案
相关题目
1.已知NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 常温常压下,1mol苯分子中含有碳氢单键数为6NA | |
| B. | 52g C2H2中含有的共用电子对数为10NA | |
| C. | 标准状况下,2.24 L乙烯和丙烯混合气体中含有5NA氢原子 | |
| D. | 标准状况下,2.24 L溴乙烷中含溴原子数目大于0.1NA |
18.下列反应中属于氧化还原反应的是( )
| A. | CO2+2NaOH═Na2CO3+H2O | B. | CuO+2HCl═CuCl2+H2O | ||
| C. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | D. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO |
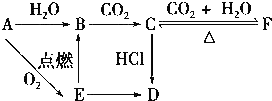
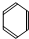 C:CH3COOH
C:CH3COOH
 的含氧官能团的名称为醚键和羧基、羟基
的含氧官能团的名称为醚键和羧基、羟基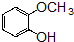
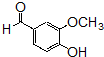 的同分异构体的结构简式
的同分异构体的结构简式