题目内容
【题目】下列元素属于海水中的常量元素的是
①H ②O ③Na ④Cl ⑤Li⑥U ⑦Ca ⑧K ⑨Br ⑩F
A. ①②③④⑦⑧⑨⑩B. ③④⑦⑧⑨⑩
C. ①②③④⑥⑦⑧⑨⑩D. ③④⑥⑦⑧⑨⑩
【答案】A
【解析】
海水中化学元素的含量差别很大。除H和O外,每千克海水中含量在1毫克以上的元素有Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、Si和F共12种,一般称为“常量元素”,故上述元素为常量元素的是①②③④⑦⑧⑨⑩,A项正确;
答案选A。

 期末宝典单元检测分类复习卷系列答案
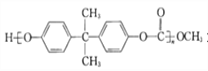
期末宝典单元检测分类复习卷系列答案【题目】中学化学中下列各物质间不能实现![]() (“→”表示一步完成)转化的是:
(“→”表示一步完成)转化的是:
A | B | C | D | |
a | CH3CH2OH | CH2===CH2 | 硬脂酸 | HCOOCH3 |
b | CH3CHO | CH3CH2Br | 硬脂酸甘油酯 | CH3OH |
c | CH3COOH | CH3CH2OH | 硬脂酸钠 | HCOOH |
A. A B. B C. C D. D
【题目】S2Cl2是工业上常用的硫化剂,已知S2C12中硫元素显+1价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂。实验室常用CS2与纯净的氯气制备S2C12。反应涉及到的几种物质的熔沸点如下:
物质 | CS2 | Cl2 | CCl4 | S2C12 |
沸点/℃ | 47 | -34.6℃ | 77 | 137 |
熔点/℃ | -109 | -100.98℃ | -23 | -77 |
实验室利用下列装置制备S2C12 (部分夹持仪器己略去):
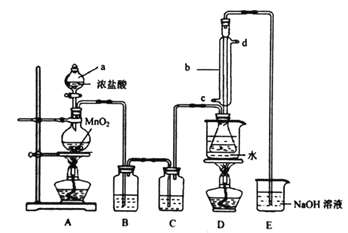
回答下列问题:
(1)装置中b玻璃仪器的名称为_______;写出制备S2C12的化学方程式_______。
(2)整套装置装配完毕后,首先进行的操作是________,再添加试剂。
(3)实验中盐酸试剂通常采用36.5%的浓盐酸,不用稀盐酸的理由是________。
装置A中反应的离子方程式是___________。
(4) D中采用热水浴加热的原因是__________,反应结束后从锥形瓶内混合物中分离出产品的方法是_______________。
(5)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因化学方程式表示为__________。
(6)该实始装置设计存在缺陷,你的改进建议及改进目的是_______________。