题目内容
【题目】(1)写出下列过程的化学方程式:
①CH3COOCH=CH2![]() A
A![]() B
B
聚合反应:______________________________________________
水解反应:_________________________________________________
②甘氨酸与盐酸反应:____________________________
(2)聚碳酸酯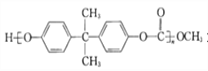 的透光率良好,可制作车、船、飞机的挡风玻璃等。原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯
的透光率良好,可制作车、船、飞机的挡风玻璃等。原来合成聚碳酸酯的一种原料是有毒的光气(COCl2),现在改用绿色化学原料碳酸二甲酯![]() 与___________(填字母序号)缩合聚合而成。
与___________(填字母序号)缩合聚合而成。
a.二卤代物 b.二酚类 c.二醛类 d.二烯类
【答案】 ![]()
![]()
![]()
![]() +n CH3COOH;
+n CH3COOH; ![]() b
b
【解析】(1)①CH3COOCH=CH2 中含有碳碳双键,可以发生加聚反应,反应方程式为![]() ,
,![]() 中含有酯基可以水解,反应的方程式为
中含有酯基可以水解,反应的方程式为![]()
![]()
![]() +n CH3COOH,故答案为:
+n CH3COOH,故答案为:![]() ,
,![]() ;
;![]()
![]()
![]() +n CH3COOH;
+n CH3COOH;
②甘氨酸与盐酸反应的方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)聚碳酸酯![]() 的单体可以为碳酰氯与
的单体可以为碳酰氯与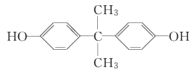 发生缩聚反应生成,也可由
发生缩聚反应生成,也可由![]() 和
和 发生缩聚反应生成,
发生缩聚反应生成, 属于二酚类物质,故选b。
属于二酚类物质,故选b。

练习册系列答案
相关题目