题目内容
已知下列顺序,其中错误的是( )
| A.氢化物稳定性增强:HF、H2O、NH3 | B.酸性减弱:HClO4、HBrO4、HIO4 |
| C.还原性增强:A1、Mg、Na | D.非金属性减弱:Cl、S、P |
A
试题分析:因为电负性为F>O>N,故氢化物稳定性减弱为:HF、H2O、NH3,所以A错误,为本题的正确答案;酸性减弱为HClO4、HBrO4、HIO4,故B正确;还原性增强为:A1、Mg、Na,故C正确;非金属性减弱为Cl、S、P,所以本题的答案选择A。
点评:本题考查了元素周期率,该考点是高考考查的重点和难点,本题有一定的综合性,但是难度不大。本题要掌握元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;元素的非金属性越强,对应的氢化物越稳定。

练习册系列答案
相关题目
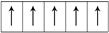 ,而不排布成
,而不排布成 ,其最直接的根据是
,其最直接的根据是
