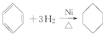题目内容
9.已知甲烷(CH4)燃料电池,用KOH溶液作电解质,则:(1)负极电极反应式:CH4+10OH--8e-═CO32-+7H2O
(2)正极电极反应式:O2+2H2O+4e-═4OH-
(2)总反应式:CH4+2O2+2OH-═CO32-+3H2O.
分析 甲烷碱性燃料电池中,甲烷在负极失电子发生氧化反应生成碳酸根离子和水,正极上氧气得电子发生还原反应生成氢氧根离子,总反应就是甲烷燃烧,据此分析.
解答 解:(1)甲烷碱性燃料电池中,甲烷在负极失电子发生氧化反应生成碳酸根离子和水,电极反应式为CH4+10OH--8e-═CO32-+7H2O,
故答案为:CH4+10OH--8e-═CO32-+7H2O;
(2)正极上氧气得电子发生还原反应生成氢氧根离子,电极反应式为O2+2H2O+4e-═4OH-,故答案为:O2+2H2O+4e-═4OH-;
(3)碱性甲烷燃料电池生成物为碳酸根离子和水,反应方程式为CH4+2O2+2OH-═CO32-+3H2O,故答案为:CH4+2O2+2OH-═CO32-+3H2O.
点评 本题考查了甲烷燃料电池中电极反应式的书写以及总化学方程式的书写,注意电解质溶液的环境决定生成物,题目难度不大.

练习册系列答案
相关题目
16.下列除杂质的方法不正确的是( )
| A. | 氢氧化铁胶体中的铁离子和氯离子可用渗析法除去 | |
| B. | 氯化钠中有少量氯化铵,加过量的烧碱溶液后加热蒸干 | |
| C. | 乙酸乙酯中混有少量乙酸,用饱和碳酸钠溶液洗涤后分液 | |
| D. | 硬脂酸甘油酯中混有少量的甘油,用盐析法除去 |
4.下列叙述正确的是( )
| A. | 在同温同压下,相同体积的任何气体所含的原子数相同 | |
| B. | 相同条件下,N2和O2的混合气体与等体积的N2所含原子数相等 | |
| C. | 等物质的量的NH4+和OH-所含质子数相等且电子数也相等 | |
| D. | 1mol 乙基中含有的电子数为18NA |
18.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L水中 | |
| B. | 10g NaOH溶解在水中配成250mL溶液 | |
| C. | 从100mL 10mol•L-1的浓盐酸中取出10mL | |
| D. | 将22.4L氯化氢气体溶于水配成1L溶液 |
19.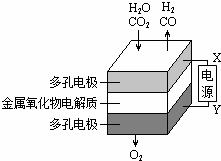 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ=H2+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2=H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
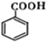 、
、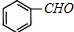 ;
;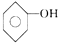 、
、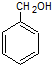 .
.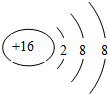 .
.