题目内容
11. Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中半径最小的元素,W与Y组成的化合物是温室气体、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中半径最小的元素,W与Y组成的化合物是温室气体、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.(1)Y2 的化学式是O2
(2)用电子式表示WQ4的形成过程
 .
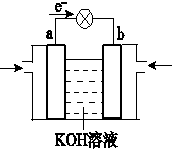
.(3)Q2与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是H2+2OH--2e-=2H2O.
(4)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是Na3N+4H2O=3NaOH+NH3•H2O.
分析 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;
Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;
W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,再结合原子结构、化学平衡、原电池原理解答.
解答 解:Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,则Y是O元素、Z是Na元素;Q与W组成的化合物是一种温室气体,Q的原子序数小于W,该气体是甲烷,则Q是H元素、W是C元素;W与Y、X与Y组成的化合物是机动车排出的大气污染物,且X的原子序数大于W而小于Y,所以X是N元素,
(1)Y为O元素,则Y2为O2,故答案为:O2;
(2)WQ4为CH4,甲烷为共价化合物,分子中存在4个碳氢键,用电子式表示甲烷的形成过程为: ,
,
故答案为: ;
;
(3)Q2为H2、Y2为O2,H2与O2的反应可将化学能转化为电能,根据电子流向知,a是负极、b是正极,a电极上通入H2,H2失电子和氢氧根离子反应生成水,电极反应式为:H2+2OH--2e-=2H2O,
故答案为:H2+2OH--2e-=2H2O;
(4)X和Z组成的一种离子化合物,能与水反应生成两种碱,则该物质是Na3N,Na3N和水反应生成氢氧化钠和一水合氨,所以该反应的化学方程式为:Na3N+4H2O=3NaOH+NH3•H2O,故答案为:Na3N+4H2O=3NaOH+NH3•H2O.
点评 本题考查了位置结构性质的相互关系及应用,题目难度中等,合理推断各元素为解答关键,注意明确原电池原理及其应用,熟练掌握原子结构与元素周期表、元素周期律的关系.

| A. | 前者大 | B. | 后者大 | C. | 一样大 | D. | 无法判断 |
| A. | CH3(CH2)2CH3 | B. | CH3(CH2)15CH3 | C. | CHCl3 | D. | CH4 |
| A. | 是乙烯的同系物 | B. | 是苯的同系物 | C. | 属于脂肪烃 | D. | 属于芳香烃 |



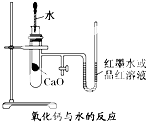 如图是某同学设计的放热反应的观察装置,其实验操作是:
如图是某同学设计的放热反应的观察装置,其实验操作是: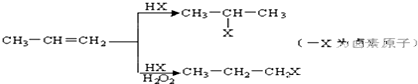
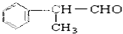 的物质,它是一种香料.
的物质,它是一种香料.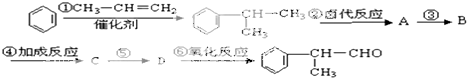
 .
. .
. .
.