题目内容
19.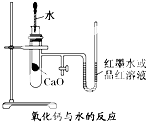 如图是某同学设计的放热反应的观察装置,其实验操作是:
如图是某同学设计的放热反应的观察装置,其实验操作是:①按图所示将实验装置连接好;
②在U形管内加入少量红墨水(或品红溶液)打开T形管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹;
③在中间的试管里盛1g氧化钙,当滴入2mL左右的蒸馏水后,即可观察.
试回答:
(1)实验中观察到的现象是U形管里的红墨水(或品红溶液)会沿开口端上升,即液面左侧下降,右侧升高.
(2)该实验中必须进行的一步实验操作是检查装置气密性.
(3)该实验的原理是CaO和H2O反应放出热量使大试管中空气膨胀,引起红墨水(或品红溶液)在U形管中的位置左低右高.
(4)实验中发生的化学反应方程式:CaO+H2O═Ca(OH)2.
(5)说明CaO、H2O的能量与Ca(OH)2能量之间的关系:CaO和H2O的能量之和大于Ca(OH)2的能量.
(6)若该实验中CaO换成NaCl,实验还能否观察到相同现象?否(填“能”或“否”).
分析 (1)氧化钙和水之间的反应是放热的,气体具有热胀冷缩的性质;
(2)由于气压原因导致的实验现象一定要保证装置不漏气;
(3)根据实验所用药品的性质以及气体热胀冷缩的性质来回答;
(4)CaO和水反应的化学反应生成Ca(OH)2;
(5)根据反应物总能量和生成物总能量之间的大小关系决定反应的吸放热情况;
(6)氯化钠和水混合后,能量的变化很不明显.
解答 解:(1)氧化钙和水之间的反应是放热的,所以试管内温度升高,气体具有热胀冷缩的性质,导致内部压强增大,U形玻璃管里的红墨水(或品红)会沿开口端上升,
故答案为:U形管里的红墨水(或品红溶液)会沿开口端上升,即液面左侧下降,右侧升高;
(2)该实验是由于气压原因导致的实验现象出现,所以实验之前一定要检查装置气密性,
故答案为:检查装置气密性;
(3)CaO和水反应放出热量,使大试管中空气膨胀,内部压强增大,引起红墨水(或品红)在U形管中的液面不再相平,
故答案为:CaO和H2O反应放出热量使大试管中空气膨胀,引起红墨水(或品红溶液)在U形管中的位置左低右高;
(4)CaO和水反应生成氢氧化钙,反应的化学反应方程式为:CaO+H2O═Ca(OH)2,
故答案为:CaO+H2O═Ca(OH)2;
(5)CaO+H2O═Ca(OH)2,根据实验现象知道:氧化钙和水之间的反应是放热的,CaO和H2O的能量和大于Ca(OH)2的能量,
故答案为:CaO和H2O的能量和大于Ca(OH)2的能量;
(6)氯化钠和水混合后,其能量的变化很不明显,试管内气体压强几乎不变,不会出现任何现象,故答案为:否.
点评 本题通过实验形式来探究放热反应,题目难度中等,可以根据所学知识来回答,注意知识的迁移和应用是关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,电极铝和镁都已除去表面氧化膜.当两装置电路中通过的电子都是1mol时,下列说法不正确的是( )| A. | 溶液的质量减小程度:乙<甲 | |
| B. | 溶液的导电能力变化:甲>乙 | |
| C. | 甲中阴极和乙中镁电极上析出物质质量:甲=乙 | |
| D. | 电极反应式:甲中阳极:2Cl--2e→Cl2↑,乙中正极:Cu2++2e→Cu |
| A. | 硝酸工业发达 | B. | 雷雨天气多 | C. | 机动车辆过多 | D. | 燃料以煤为主 |
| A. | 元素周期表是元素按原子序数从小到大从左到右排列而成的 | |
| B. | 主族元素原子的电子层数等于其所在周期的周期序数 | |
| C. | 四、五、六周期中都含有18种元素,其中Ⅷ族中所含元素种类最多 | |
| D. | 元素周期表中有18列、16个族,且第二列中无非金属元素 |
| A. | NH3的电子式: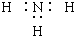 | |
| B. | 氯气的化学式:Cl | |
| C. | 氮气的电子式: | |
| D. | 硫酸铝的电离方程式:Al2(SO4)3═Al3++SO42- |
| A. | 同分异构体 | B. | 同系物 | C. | 同一物质 | D. | 同一类物质 |
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| C. | 生石灰能与水反应,可用来干燥氯气 | |
| D. | 从海水中提取物质都必须通过化学反应才能实现 |
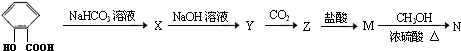
 Y
Y M
M N
N
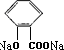 +CO2+H2O→
+CO2+H2O→ +NaHCO3.
+NaHCO3.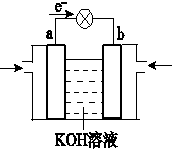 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中半径最小的元素,W与Y组成的化合物是温室气体、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中半径最小的元素,W与Y组成的化合物是温室气体、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物. .
.