题目内容
3.下列物质能促进水的电离的是( )| A. | CH3COONa | B. | Ba(OH)2 | C. | H2SO4 | D. | KNO3 |
分析 水为弱电解质,能够电解出氢离子和氢氧根离子,在溶液中存在电离平衡;加入酸溶液和碱溶液能够抑制水的电离,加入能够水解的盐促进了水的电离,据此进行判断.
解答 解:A、醋酸钠为强碱弱酸盐,醋酸根离子结合水电离的氢离子,水的电离程度增大,醋酸钠促进了水的电离,故A正确;
B、加入氢氧化钡引入了大量的OH-,氢氧根的浓度增大,对水的电离有抑制作用,故B错误;
C、加入硫酸,溶液中氢离子浓度增大,水的电离平衡向着逆向移动,抑制了水的电离,故C错误;
D、加入硝酸钾是强酸强碱的正盐,既不能水解又不能电离出H+或OH-,对水的电离无影响,故D错误;
故选A.
点评 本题考查了水的电离及其影响因素,题目难度不大,注意掌握水的电离及影响,明确酸碱溶液抑制水的电离,含有弱酸根或者弱碱根离子的盐能够促进水的电离.

练习册系列答案
相关题目
14.短周期元素X,Y,Z,W,Q在元素周期表中的相应位置如下表所示,下列说法错误的是( )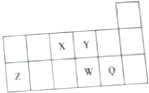

| A. | X的最高价氧化物对应水化物能与它的氢化物反应 | |
| B. | Y原子的电子总数是其K层电子数的3倍 | |
| C. | Z的氧化物能溶于氢氧化钠溶液 | |
| D. | Q的单质能与W的氢化物发生置换反应 |
18.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的A为无色粘稠液体,易溶于水.为研究A的组成与结构,进行实验如表所示:
| 实验步骤 | 解释或实验结论 |
| (1)称取A9.0g,升温使其变化,测其密度是相同条件下H2的45倍 | (1)A的相对分子质量为90 |
| (2)将此9.0gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g | (2)A的分子式为C3H6O3 |
| (3)另取A9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况) | (3)用结构简式表示A中含有的官能团羧基、羟基 |
(4)A的核磁共振氢谱如图: | (4)综上所述,A的结构简式为 |
(5)已知两分子A在一定条件下可生成六元环状酯,写出该反应的化学方程式:2 $→_{△}^{浓硫酸}$ $→_{△}^{浓硫酸}$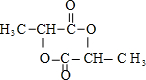 +2H2O. +2H2O. | |
8.下列措施可以促进明矾水解的是 ( )
| A. | 加H2SO4 | B. | 加NH4Cl | C. | 加热 | D. | 加压 |
15.下列关于分散系的说法错误的是( )
| A. | 溶液、胶体、浊液属于不同的分散系 | |
| B. | 胶体与其他分散系的本质区别是分散质粒子直径的大小 | |
| C. | 可利用丁达尔现象鉴别溶液和胶体 | |
| D. | 利用过滤的方法可以分离胶体和溶液 |
12.对于工业合成氨反应:N2+3H2?2NH3,下列说法不正确的是( )
| A. | 增大压强可以加快反应速率 | |
| B. | 升高温度可以加快反应速率 | |
| C. | 增大N2浓度可以使H2转化率达到100% | |
| D. | 合成氨反应的限度可以随着条件的改变而改变 |
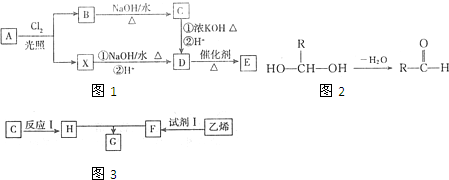
 ,C中官能团的名称是醛基;
,C中官能团的名称是醛基;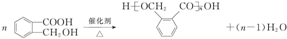 ;
;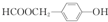 ;
;
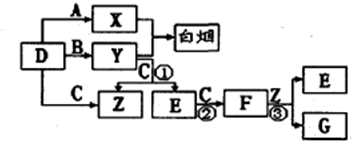 A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题:
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题: