题目内容
17.氮和钠可形成化合物Na3N,它能与水剧烈反应产生NH3,下列叙述正确的是( )| A. | Na3N与水的反应是氧化还原反应 | |
| B. | Na3N 是共价化合物 | |
| C. | Na3N中4个离子均满足最外层8电子稳定结构 | |
| D. | Na3N中钠离子半径大于氮离子半径 |
分析 Na3N是离子化合物,由Na+和N3-构成,根据离子的结构可知,电子层数相同,所以半径大小取决于核电荷数,核电荷数越大,离子半径越小;离子化合物中不存在共价键;该化合物与水反应生成NaOH和NH3可知是氮化纳发生的剧烈的水解反应,反应前后元素化合价没有变化,所以不是氧化还原反应.
解答 解:A、Na3N与水的反应为,Na3N+H2O=NaOH+NH3↑,反应前后各元素化合价没变化,不是氧化还原反应,故A错误;
B、Na3N是有三个钠离子和一个氮离子构成,存在离子键,不存在共价键,是离子化合物,故B错误;
C、Na3N中钠离子和氮离子的电子层数相同,均含有10个电子,则4个离子均满足最外层8电子稳定结构,故C正确;
D、Na3N中钠离子和氮离子的电子层数相同,电子层数相同离子半径由核电荷数决定,核电荷数越大,离子半径越小,所以钠离子半径小于氮离子半径,故D错误;
故选C.
点评 本题考查了离子半径的大小比较,离子化合物的构成特征,水解的反应过程,主要考查了信息应用的能力.

练习册系列答案
相关题目
13.下列有机化合物既可以通过取代反应,也可以通过加成反应或水解反应制得的是( )
| A. | 乙烷 | B. | 乙酸乙酯 | C. | 乙醇 | D. | 葡萄糖 |
5.300℃时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
回答下列问题:
(1)反应0~2min Z的平均速率v(Z)=0.004 mol/(L•min)
(2)能判断该反应已经达到平衡状态的是D
A.生成X的速率是生成Z的速率的2倍 B.容器内压强保持不变
C.容器内气体的密度保持不变 D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是降低温度(任写一种).
(4)温度为300℃时,该反应的化学平衡常数K=1.44
(5)若起始时向该容器中充入X、Y、Z各0.20mol,则反应将向正(填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比不变(填“增大”、“减小”或“不变”)
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
(1)反应0~2min Z的平均速率v(Z)=0.004 mol/(L•min)
(2)能判断该反应已经达到平衡状态的是D
A.生成X的速率是生成Z的速率的2倍 B.容器内压强保持不变
C.容器内气体的密度保持不变 D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是降低温度(任写一种).
(4)温度为300℃时,该反应的化学平衡常数K=1.44
(5)若起始时向该容器中充入X、Y、Z各0.20mol,则反应将向正(填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比不变(填“增大”、“减小”或“不变”)
12.下列实验操作正确且能达到实验目的都是( )
| A. | 将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色 | |
| B. | 向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀:再加入少许浓硫酸,迅速搅拌,探究浓硫酸的吸水性 | |
| C. | 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 | |
| D. | 将表面有铜绿[Cu2(OH)2C03]的铜器放入盐酸中浸泡,除去铜绿 |

 .
.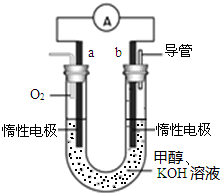 (1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是b
(1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是b
 .
.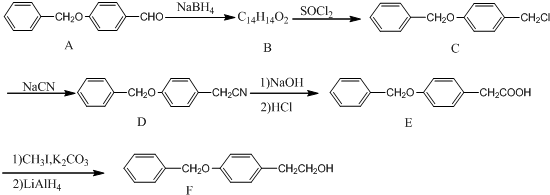
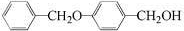 ;由A→B的反应类型是:还原反应.
;由A→B的反应类型是:还原反应.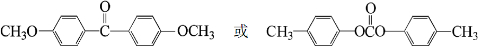 .
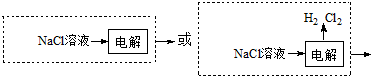
. 为原料制备化合物X(
为原料制备化合物X(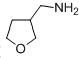 )(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
)(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如下: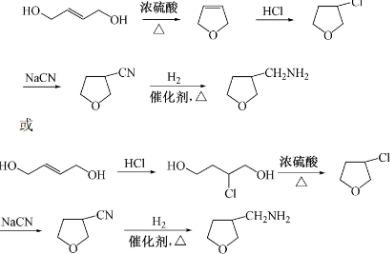 .
. .
.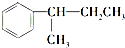 $\stackrel{酸性KMnO_{4}溶液}{→}$
$\stackrel{酸性KMnO_{4}溶液}{→}$ .
.