题目内容
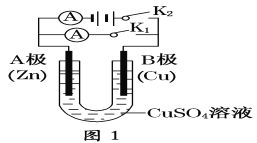
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示。

(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A |
FeCl3溶液显酸性的原因是_______________________(用离子方程式表示)。写出装置A中产生SO2的化学方程式:______________________。
(2)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔效应。将混合液放置12小时,溶液才变成浅绿色。
【资料】[Fe(HSO3)]2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成[Fe(HSO3)]2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色[Fe(HSO3)]2+的原因:_____________________。
写出溶液中[Fe(HSO3)]2+离子与Fe3+反应的离子方程式:_________________。
(3)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤②③的实验。
步骤② | 往5 mL 1 mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色 |
步骤③ | 往5 mL重新配制的1 mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色 |
用铁氰化钾K3[Fe(CN)6] 溶液检验步骤②和步骤③所得溶液中的Fe2+,其现象为______________
(4)综合上述实验探究过程,可以获得的实验结论:
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物[Fe(HSO3)]2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.______________________ _______。
【答案】(1)Fe3++3H2O![]() Fe(OH)3+3H+(2分)
Fe(OH)3+3H+(2分)
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O(2分)
CuSO4+SO2↑+2H2O(2分)
(2)Fe3++H2O+SO2![]() [Fe(HSO3)]2++H+
[Fe(HSO3)]2++H+
(或者SO2+H2O![]() H2SO3,H2SO3
H2SO3,H2SO3![]() HSO3-+H+Fe3++HSO3-
HSO3-+H+Fe3++HSO3-![]() [Fe(HSO3)]2+)(3分)
[Fe(HSO3)]2+)(3分)
Fe3++H2O+[Fe(HSO3)]2+===2Fe2++SO![]() +3H+(2分)
+3H+(2分)
(3)生成蓝色沉淀(2分)(4)加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间(2分)
【解析】
试题分析:(1)氯化铁是强酸弱碱盐,铁离子水解溶液显酸性,方程式为Fe3++ 3H2O![]() Fe(OH)3+ 3H+ 。在加热的条件下浓硫酸与铜发生氧化还原反应生成SO2,反应的化学方程式为Cu + 2H2SO4(浓)
Fe(OH)3+ 3H+ 。在加热的条件下浓硫酸与铜发生氧化还原反应生成SO2,反应的化学方程式为Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+2H2O。
CuSO4 + SO2↑+2H2O。
(2)SO2溶于水生成亚硫酸,亚硫酸是二元弱酸,电离出亚硫酸氢根离子,亚硫酸氢根离子结合铁离子生成Fe(HSO3)2+,生成Fe(HSO3)2+离子可以将Fe3+还原为Fe2+,有关反应的离子方程式为H2O+SO2![]() H2SO3、H2SO3
H2SO3、H2SO3 ![]() H++HSO3-、Fe3++HSO3-
H++HSO3-、Fe3++HSO3-![]() Fe(HSO3)2+、Fe3++H2O+Fe(HSO3)2+===2Fe2++SO42-+3H+。
Fe(HSO3)2+、Fe3++H2O+Fe(HSO3)2+===2Fe2++SO42-+3H+。
(3)铁氰化钾溶液与亚铁离子结合可以产生蓝色沉淀,所以实验现象为生成蓝色沉淀。
(4)根据步骤②③中的实验现象可以推测其第三个结论是加热、提高FeCl3溶液的酸性会缩短浅绿色出现的时间。