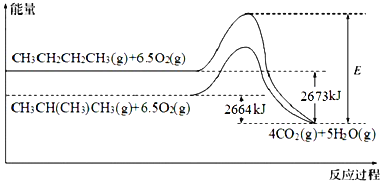
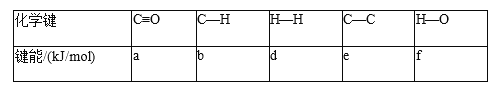
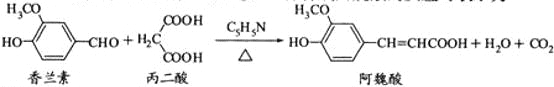��Ŀ����
����Ŀ��Ԫ��X��Y��Z��M��R��Ϊ����������Ԫ�أ���ԭ����������������֪��YΪ�ؿ��к�������Ԫ�أ�Mԭ�ӵ��������������������֮��Ϊ3��4��R-��Z+��X+���Ӱ뾶��С��������XR������Ϊ���壬��ش��������⣺
��1��M��Ԫ�����ڱ��е�λ��__��Z+���ӵĽṹʾ��ͼΪ__��
��2��д��X��Y��R��ԭ�Ӹ���֮��1��1��1�γɵĻ�����ĵ���ʽ__��
��3��X��Y�ɷֱ��γ�10���Ӻ�18���ӵķ��ӣ�д����18���ӷ���ת����10���ӷ��ӵĻ�ѧ����ʽ__��
��4��ʵ�����Ʊ�R�ĵ��ʣ��÷�Ӧ�����ӷ���ʽΪ__��
��5��R�ǽ�����ǿ��M������ѡ������֤����һ��ʵ����__(����ĸ���)��
A.�����µ�R�����۷е��M���ʵĸ�
B.R���⻯���M���⻯����ȶ�
C.һ��������R��M�ĵ��ʶ�����NaOH��Һ��Ӧ
D.����������Ӧˮ���������ǿ����R>M
��6����X��Y��Z��M����Ԫ����ɵ�һ��������ʽ��A����A��Һ��ͨ���������õ���ɫ��Һ��д���÷�Ӧ�����ӷ���ʽ__��
���𰸡���3���ڵ�VIA�� Na+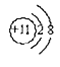
![]() 2H2O2
2H2O2![]() 2H2O+O2�� MnO2+4H++2Cl-
2H2O+O2�� MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O BD HSO3-+H2O+Cl2=SO42-+2Cl-+3H+
Mn2++Cl2��+2H2O BD HSO3-+H2O+Cl2=SO42-+2Cl-+3H+
��������
YΪ�ؿ��к�������Ԫ�أ���YΪO��Mԭ�ӵ��������������������֮��Ϊ3��4����MΪS��R-����ΪF-��Cl-��Z+ ��X+����ΪH+��Li+��Na+��R-��Z+��X+���Ӱ뾶��С��Ԫ��X��Y��Z��M��R��Ϊ����������Ԫ�أ���ԭ����������������RΪCl��XΪH��ZΪNa��
��1��MΪS����Ԫ�����ڱ��е�λ��Ϊ��3���ڵ�VIA�壻ZΪNa ��Z+���ӵĽṹʾ��ͼΪ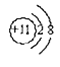 ���ʴ�Ϊ����3���ڵ�VIA�壻
���ʴ�Ϊ����3���ڵ�VIA�壻 ��
��
��2��XΪH ��YΪO��RΪCl����ԭ�Ӹ���֮��1��1��1�γɵĻ�������HClO�������ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��3��XΪH ��YΪO���γ�10���ӵķ���ΪH2O��18���ӵķ���ΪH2O2��H2O2ת����H2O�Ļ�ѧ����ʽΪ��2H2O2![]() 2H2O+O2�����ʴ�Ϊ��2H2O2
2H2O+O2�����ʴ�Ϊ��2H2O2![]() 2H2O+O2����
2H2O+O2����
��4��RΪCl��ʵ�����ö������̺�Ũ�����Ʊ�Cl2�������ӷ�Ӧ����ʽΪ��MnO2+4H++2Cl-![]() Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+
Mn2++Cl2��+2H2O���ʴ�Ϊ��MnO2+
4H++2Cl-![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
��5��A. �����µ�Cl2���۷е��S�ĸߣ�����˵��Cl2�ķǽ����Ա�S��ǿ��A����
B. �ǽ�����Խǿ�����⻯��Խ�ȶ���Cl2���⻯���S���⻯����ȶ�����˵��Cl2�ķǽ����Ա�S��ǿ��B��ȷ��
C. һ��������Cl2��S�Ķ�����NaOH��Һ��Ӧ������˵��
D. �ǽ�����Խǿ��������������Ӧˮ���������Խǿ������������Ӧˮ���������ǿ����HClO4>H2SO4��˵��Cl2�ķǽ����Ա�S��ǿ��D��ȷ���ʴ�Ϊ��BD��
��6��XΪH ��YΪO��MΪS��ZΪNa����������Ԫ����ɵ�һ��������ʽ��ΪNaHSO3����������Ӧ�����ӷ���ʽΪ��HSO3-+H2O+Cl2=SO42-+2Cl-+3H+���ʴ�Ϊ��HSO3-+H2O+Cl2=SO42-+2Cl-+3H+��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ���ú�﮷�������Ҫ����Ԫ�صĺ�����Li 3.50% Ni 6.55% Ca 6.41% Mg 13.24%)�Ʊ�Li2CO3,�������Ʊ�﮵�ص���������LiFePO4�����ֹ����������£�
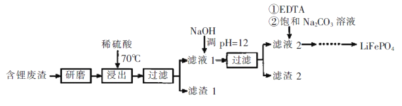
���ϣ�i��Һ1����Һ2�в�������Ũ�ȣ�g��L��1��
Li�� | Ni2�� | Ca2�� | Mg2�� | |
��Һ1 | 22.72 | 20.68 | 0.36 | 60.18 |
��Һ2 | 21.94 | 7.7��10��3 | 0.08 | 0.78��10��3 |
ii��EDTA�ܺ�ijЩ���۽��������γ��ȶ���ˮ���������
iii��ijЩ���ʵ��ܽ�ȣ�S��
T/�� | 20 | 40 | 60 | 80 | 100 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
S(Li2SO4)/g | 34.7 | 33.6 | 32.7 | 31.7 | 30.9 |
I.�Ʊ�Li2CO3��Ʒ
��1������������Ϊ�ӿ컯ѧ��Ӧ���ʶ���ȡ�Ĵ�ʩ��____��
��2������2����Ҫ�ɷ���____��
��3������Һ2���ȼ���EDTA,�ټ��뱥��Na2C03��Һ,90���ַ�Ӧ��������� Li2CO3��Ʒ�IJ�����_______��
��4������lkg���3.50%�ķ�����﮵Ľ�����Ϊa��Li+ת��ΪLi2CO3��ת����Ϊb�����Ʒ�к�Li2CO3��������________g����Ħ������:Li2CO3 74 g.mol4)
II.����Li2CO3��Ʒ
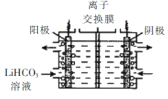
��5����Li2CO3ת��ΪLiHCO3���ø�Ĥ�����LiHCO31��Һ�Ʊ��ߴ��ȵ�LiOH,��ת���õ�ؼ�Li2CO3�����ԭ����ͼ��ʾ�������ĵ缫��Ӧʽ��____,�ó�ʹ����_________(���������������������ӽ���Ĥ��
��.�Ʊ� LiFePO4
��6������ؼ�Li2CO3��C��FePO4�����·�Ӧ������LiFePO4��һ�ֿ�ȼ������,�÷�Ӧ�Ļ�ѧ����ʽ��_________��
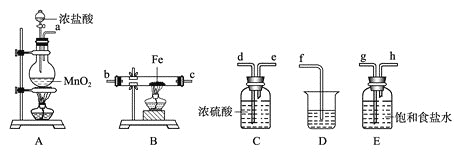
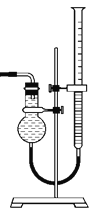
����Ŀ������������������۷���Ϣ�صijɷ�֮һ�������㽶����ζ��ʵ�����Ʊ������������ķ�Ӧ��װ��ʾ��ͼ���й��������£�
![]()
��Ŀ | ��Է������� | �ܶ�/(g��cm3) | �е�/�� | ˮ���ܽ��� |
���촼 | 88 | 0.8123 | 131 | �� |
���� | 60 | 1.0492 | 118 | �� |
���������� | 130 | 0.8670 | 142 | ���� |
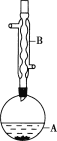
ʵ�鲽�裺
��A�м���4.4g���촼��6.0g���ᡢ����Ũ�����2��3Ƭ���Ƭ����ʼ��������A������50min����ӦҺ�������º����Һ©���У��ֱ�������ˮ������̼��������Һ��ˮϴ�ӣ��ֳ��IJ������������ˮMgSO4���壬����Ƭ�̣����˳�ȥMgSO4���壬�����������ռ�140��143����֣�������������3.9g��
�ش��������⣺
��1������B��������___��
��2����ϴ�Ӳ����У���һ��ˮϴ�͵ڶ���ˮϴ����ҪĿ�ķֱ���___��
��3����ϴ�ӡ���Һ�����У�Ӧ�����Ȼ���ã����ֲ��__(����)��
a.ֱ�ӽ������������ӷ�Һ©�����Ͽڵ���
b.ֱ�ӽ������������ӷ�Һ©�����¿ڷų�
c.�Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ��������������¿ڷų�
d.�Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ��������������Ͽڵ���
��4��ʵ���м���������ˮMgSO4��Ŀ����___��
��5����ʵ��IJ�����___(����)��
a.30% b.40% c.60% d.90%