题目内容
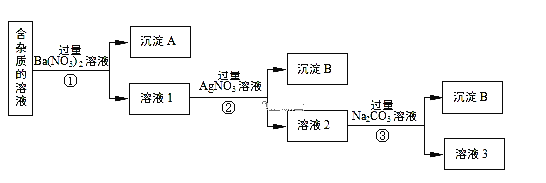
【题目】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
(1)沉淀A的主要成分是__________________________(填化学式)。
(2)②中反应的离子方程式是___________________________________________。
(3)①②③中均进行的分离操作是_______________。
(4)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是__________,为了除去杂质,可向溶液3中加入适量的______________。
(5)实验室用上述实验获得的NaNO3固体配制450 mL 0.40 mol/L NaNO3溶液。该同学需称取NaNO3固体的质量是________ g。
(6)下面是该同学配制过程的示意图,其操作中有错误的是(填操作序号)___________。
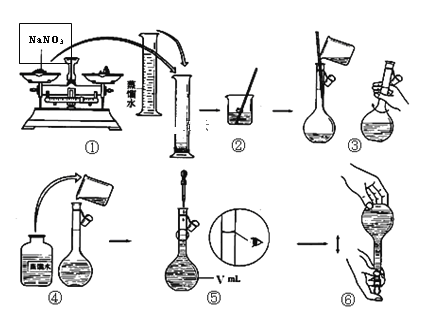
第⑤部操作可能会使所配溶液浓度偏_______(填“大”或“小”或“无影响”)
【答案】BaCO3、BaSO4 Ag+ + Cl-= AgCl↓ 过滤 Na2CO3 稀HNO3 17.0 ①、④、⑤ 小
【解析】
(1)含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液中加入过量的Ba(NO3)2,Na2SO4、Na2CO3和Ba(NO3)2反应生成BaSO4、BaCO3沉淀;
(2)滤液1中含氯离子,加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,反应的离子方程式为:Ag++Cl-═AgCl↓;
(3)①②③中均进行的分离是把不溶性物质和可溶性物质分离,故为过滤;
(4)溶液3为NaNO3和Na2CO3的混合物,加入稀HNO3,可除去Na2CO3,最后加热蒸发、冷却结晶、过滤得到硝酸钠,故答案为:Na2CO3;HNO3;
(5)实验室没有450 mL规格的容量瓶,必须配制500mL,制备500mL 0.4mol/L的NaNO3溶液,则需要硝酸钠的质量为0.5L×0.4mol/L×85g/mol=17.0g;
(6)①硝酸钠应该放在纸片上或玻璃片上称量,①不正确;向容量瓶中加入蒸馏水时,应该用玻璃棒引流,④错误;定容时应该平视,⑤不正确,所以答案选①④⑤;
②第⑤步操作可能会使所配溶液浓度偏定容时仰视刻度线,体积偏大,浓度偏小。