题目内容
9.断裂以下的物质需要能量最多的是( )| A. | HCl | B. | HBr | C. | HI | D. | HAt |
分析 键能是指拆开1mol共价键所需要吸收的能量,键长与形成共价键的原子的半径有关,原子半径越大,键长越长,键能越小,断裂以下的物质需要能量最多指键能最大.
解答 解:HCl;HBr;HI、HAt结构相似,氢原子半径相等,氯溴碘砹中氯的原子半径最小,H-Cl键长最短,键能最大,断裂需要能量最多,
故选A.
点评 本题考查键能与键长的关系,题目难度不大,注意键长与形成共价键的原子的半径有关,原子半径越大,键长越长,键能最大,断裂需要能量最多.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
20.下列有关铝的化合物的说法正确的是( )
| A. | 氧化铝坩埚可用于熔融NaOH实验 | |
| B. | 氧化铝的熔点很高,是一种较好的耐火材料 | |
| C. | 明矾可用于自来水的消毒 | |
| D. | 氢氧化铝能中和胃酸,适合于胃溃疡患者服用 |
4.下列说法中正确的是( )
| A. | FeCl3 溶液和Fe(OH)3 胶体外观均是透明液体. | |
| B. | 制备Fe(OH)3 胶体的方法是将饱和FeCl3 溶液加热煮沸 | |
| C. | 28gCO和C2H4混合气体含有的分子数为2NA | |
| D. | 溶液和胶体的本质区别是丁达尔效应 |
1.由两种金属组成的合金8g,投入到足量的稀硫酸中,测得产生气体5.6L(标准状况),则原合金不可能是( )
| A. | Mg-Cu合金 | B. | Mg-Fe合金 | C. | Al-Zn合金 | D. | Fe-Zn合金 |
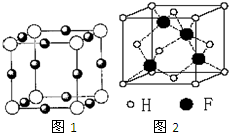 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)