题目内容
13.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂也不是还原剂.下列反应与Cl2+SO2+2H2O=H2SO4+2HCl相比较,水的作用完全相同的是( )| A. | 2H2O $\frac{\underline{\;电解\;}}{\;}$ 2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2Na+2H2O=2NaOH+H2↑ | D. | Cl2+H2O=HCl+HClO |
分析 Cl2+SO2+2H2O=H2SO4+2HCl中,Cl、S元素的化合价变化,则水既不是氧化剂也不是还原剂,以此来解答.
解答 解:A.水中O元素的化合价升高,氢化合价降低,则既是氧化剂又是还原剂,故A不选;
B.Fe、O化合价变化,水中各元素的化合价变化,则水既不是氧化剂也不是还原剂,故B选;
C.水中H元素的化合价降低,水为氧化剂,故C不选;
D.只有Cl元素的化合价变化,水中各元素的化合价变化,则水既不是氧化剂也不是还原剂,故D选;
故选BD.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意常见元素的化合价,题目难度不大.

练习册系列答案
相关题目
3.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 12g石墨和C60的混合固体中,含NA个碳原子 | |
| B. | 标准状况下,2.24L水中含有0.1NA个水分子 | |
| C. | 7.8g过氧化钠含有的阴离子数为0.2NA | |
| D. | 0.1mol铁在足量氯气中燃烧,电子转移数目为0.2NA |
5.下列物质属于天然高分子化合物的是( )
| A. | 淀粉 | B. | 蔗糖 | C. | 油脂 | D. | 葡萄糖 |
9.实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
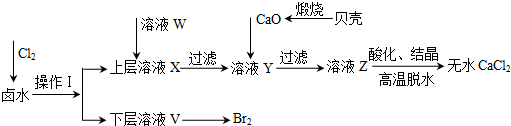
(1)操作Ⅰ使用的试剂是四氯化碳,所用的主要仪器名称是分液漏斗.
(2)加入溶液W的目的是除去溶液中的SO42-.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是11.0≤pH<12.2.酸化溶液Z时,使用的试剂为盐酸.

(1)操作Ⅰ使用的试剂是四氯化碳,所用的主要仪器名称是分液漏斗.
(2)加入溶液W的目的是除去溶液中的SO42-.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是11.0≤pH<12.2.酸化溶液Z时,使用的试剂为盐酸.
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol•L-1 |