题目内容
3.下列说法正确的是(NA表示阿伏加德罗常数的值)( )| A. | 1mol N2中含有的电子数为2NA | |
| B. | 标准状态下,1mol水所含的氧原子数为1NA | |
| C. | 常温常压下,17g氨气所含的分子数大于NA | |
| D. | 2g氢气所含的氢原子数为NA |
分析 A、氮气中含14个电子;
B、水中含1个氧原子;
C、氨气的分子个数N=$\frac{m}{M}{N}_{A}$;
D、氢气由氢原子构成.
解答 解:A、氮气中含14个电子,故1mol氮气中含14mol电子即14NA个,故A错误;
B、水中含1个氧原子,故1mol水中含1mol氧原子即NA个,故B正确;
C、氨气的分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{17g}{17g/mol}{N}_{A}$=NA,故C错误;
D、氢气由氢原子构成,故2g氢气中含有的氢原子的物质的量为n=$\frac{2g}{1g/mol}$=2mol,个数为2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17.用如图所示实验装置进行相应实验,能达到实验目的是( )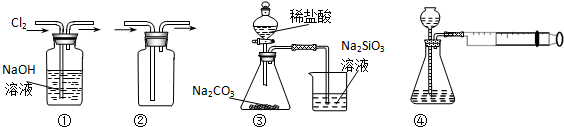

| A. | 装置①可用于除去Cl2中含有的少量HCl气体 | |
| B. | 装置④向左推动针筒活塞可检验该装置的气密性 | |
| C. | 装置③可证明非金属性Cl>C>Si | |
| D. | 按装置②所示的气流方向可用于收集H2、NH3等 |
18.前四周期主族非金属元素X、Y、Z和W在元素周期表中的相应位置如图所示,下列说法正确的是( )
| X | Y | |
| Z | W |
| A. | 元素X和元素W最高正价代数和一定为8 | |
| B. | 若元素X的原子序数为a,则Z的原子序数一定为a+9. | |
| C. | 常温下,若X的简单氢化物的水溶液能使红色石蕊试液变蓝,则元素Y的简单氢化物的沸点一定高于元素W的简单氢化物 | |
| D. | 原子半径的大小顺序为rW>rZ>rX>rY. |
11.NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1.0L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 12g石墨烯(单层石墨)中含有C-12原子的个数为NA | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA | |
| D. | 1 mol的羟基与1 moL的甲基所含电子数均为9 NA |
15.下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100ml 0.5mol/L MgCl2溶液 | B. | 200ml 0.25mol/L HCl溶液 | ||
| C. | 50ml 1mol/L NaCl溶液 | D. | 200ml 0.25mol/L CaCl2溶液 |
13.下列说法中正确的是( )
| A. | 在25℃纯水中,c(H+)=c(OH-)=10-7 mol/L,呈中性 | |
| B. | 溶液中,若c(H+)>10-7mol/L,则c(H+)>c(OH-),呈酸性 | |
| C. | c(H+)越大,则pH 越大,溶液的碱性越强 | |
| D. | pH为0的溶液,其中只有H+而无OH- |
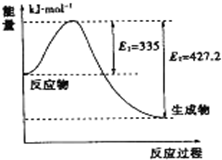 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.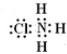 .
.