题目内容
19. 热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )
热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )| A. | 放电过程中,Li+向正极移动 | |
| B. | 常温下电解质是不导电的固体,电池不工作 | |
| C. | 每转移0.1 mol 电子,理论上生成20.7 g Pb | |
| D. | 该电池总反应为 PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb |
分析 由原电池总反应可知Ca为原电池的负极,反应的电极方程式为Ca+2Cl--2e-=CaCl2,原电池的正极,发生还原反应,电极方程式为PbSO4+2e-+2Li+=Li2SO4+Pb,原电池工作时,阳离子向正极移动,阴离子向负极移动,结合电解方程式计算.
解答 解:A.原电池工作时,阳离子向正极移动,故A正确;
B.熔融无水LiCl-KCl混合物作电解质,存在自由移动的离子,电解质是不导电的固体,无法构成原电池,故B正确;
C.根据电极方程式PbSO4+2e-+2Li+=Li2SO4+Pb,可知每转移0.1 mol电子,理论上生成0.05molPb,质量为10.35g,故C错误;
D,由原电池总反应可知Ca为原电池的负极,反应的电极方程式为Ca+2Cl--2e-=CaCl2,原电池的正极,发生还原反应,电极方程式为PbSO4+2e-+2Li+=Li2SO4+Pb,正极和负极相机可以得到总反应,即PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb,故D正确.
故选C.
点评 本题考查原电池的工作原理,注意根据总反应式结合物质所含元素化合价的变化判断原电池的正负极,把握电极方程式的书写方法,易错点为D,注意把握原电池的构成条件,题目难度中等.

练习册系列答案
相关题目
7.下列事实不能用平衡移动原理解释的是( )
| A. | 加催化剂,使N2和H2在一定条件下转化为NH3 | |
| B. | 增大压强,有利于SO2和O2反应生成SO3 | |
| C. | 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| D. | 黄绿色的氯水光照后颜色变浅 |
11.下列有关物质检验的实验结论正确的是( )
| 选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
| A | 向某溶液中加入硝酸钡溶液,有白色沉淀生成,滴入稀硝酸,沉淀未消失 | 该溶液中一定含有SO42- |
| B | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| C | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中滴入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| D | 将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 | 该物质一定属于醛类 |
| A. | A | B. | B | C. | C | D. | D |
8.实验是化学的基础.下列说法正确的是( )
| A. | 过氧化钠、氯水、浓硝酸通常都要密封保存于棕色试剂瓶中 | |
| B. | 盛溴的试剂瓶里加少量水以减少溴的挥发 | |
| C. | 钾、钠、白磷都应保存在水中 | |
| D. | 做焰色反应实验时所用铂丝,每次用完后用稀硫酸洗涤后再使用 |
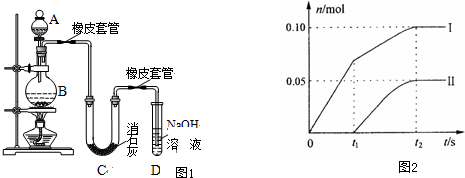


 .塑料制品是人类日常生活中使用量最大的合成高分子材料.大量塑料制品的生产和使用,给人们的生活带来了极大的方便,同时也造成了严重的环境问题--白色污染.当今白色污染问题已得到了人们应有的重视,一些科学家也成功地寻找到了治理白色污染的有效途径.结合学过的知识,回答下列问题:
.塑料制品是人类日常生活中使用量最大的合成高分子材料.大量塑料制品的生产和使用,给人们的生活带来了极大的方便,同时也造成了严重的环境问题--白色污染.当今白色污染问题已得到了人们应有的重视,一些科学家也成功地寻找到了治理白色污染的有效途径.结合学过的知识,回答下列问题: .
.