题目内容
8.实验是化学的基础.下列说法正确的是( )| A. | 过氧化钠、氯水、浓硝酸通常都要密封保存于棕色试剂瓶中 | |
| B. | 盛溴的试剂瓶里加少量水以减少溴的挥发 | |
| C. | 钾、钠、白磷都应保存在水中 | |
| D. | 做焰色反应实验时所用铂丝,每次用完后用稀硫酸洗涤后再使用 |
分析 A.过氧化钠见光不易分解;
B.液溴易挥发;
C.钾、钠均与水反应;
D.硫酸难挥发,干扰焰色反应中离子的检验.
解答 解:A.过氧化钠见光不易分解,放在无色试剂瓶即可,故A错误;
B.液溴易挥发,则盛溴的试剂瓶里加少量水以减少溴的挥发,故B正确;
C.钾、钠均与水反应,不能保存在水中,而白磷可保存在水中,故C错误;
D.硫酸难挥发,干扰焰色反应中离子的检验,则所用铂丝,每次用完后用稀盐酸洗涤后再使用,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握试剂的保存、焰色反应等为解答的关键,注意实验操作的评价性分析,侧重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19. 热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )
热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )
 热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )
热激活电池可用作火箭、导弹的工作电源.该电池以Ca为负极,熔融无水LiCl-KCl混合物作电解质,结构如下图所示.正极反应式为PbSO4+2Li++2e-=Li2SO4+Pb.下列说法不正确的是( )| A. | 放电过程中,Li+向正极移动 | |
| B. | 常温下电解质是不导电的固体,电池不工作 | |
| C. | 每转移0.1 mol 电子,理论上生成20.7 g Pb | |
| D. | 该电池总反应为 PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb |
16.下列离子方程式正确,且与所述事实相符的是( )
| A. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O | |
| B. | 向水中通氯气:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 在强碱溶液中,次氯酸钠与Fe(OH)3 反应生成Na2FeO4,离子方程式:3ClO-+2Fe(OH)3═2FeO42-+H2O+3Cl-+4H+ |
3.羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下可分解为CO和S.下列有关说法正确的是( )
| A. | OCS、CO、CO2、S四种物质的晶体类型相同 | |
| B. | OCS在高温下分解时,碳元素化合价升高 | |
| C. | OCS分子中含有2个σ键和2个π键,它们均属于非极性键 | |
| D. | 22.4 L OCS中约含有3×6.02×1023个原子 |
20.下列有机物检验方法正确的是( )
| A. | 取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 | |
| B. | 用酸性KMnO4溶液直接检验乙醇与浓硫酸反应是否得到乙烯 | |
| C. | 用燃烧的方法鉴别甲烷与苯 | |
| D. | 用新制CaO检验乙醇中是否含有水分 |
17.用KHC2O4(pKa1=1.23,pKa2=4.19)和K2C2O4配制缓冲溶液,其有效缓冲范围是( )
| A. | 0.23~2.23 | B. | 2.23~3.19 | C. | 3.19~5.19 | D. | 4.19~6.19 |
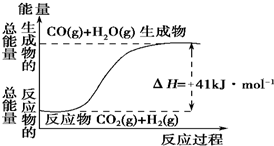 (1)根据如图所示情况,判断下列说法中正确的是B.
(1)根据如图所示情况,判断下列说法中正确的是B. 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.