题目内容
温度为T时,向2 L恒容密闭容器中充入1 mol PCl5,发生PCl5(g)  PCl3(g) + Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是
PCl3(g) + Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是
| A.反应在0 ~50 s 的平均速率v(Cl2) =1.6×10-3mol/(L·s) |
| B.该温度下,反应的平衡常数K = 0.025 |
| C.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,则该反应的ΔH <0 |
| D.反应达平衡后,再向容器中充入 1 mol PCl5,该温度下再达到平衡时,0.1 mol/L<c(Cl2)<0.2 mol/L |
C
解析试题分析:A、反应在0 ~50 s 的平均速率v(Cl2) =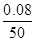 = 1.6×10-3 mol/(L·s),正确;B、平衡时C(Cl2)=0.1mol/L=C(PCl3),C(PCl5)=0.4mo/L,K = 0.025,正确;C升高温度,平衡时c(PCl3)=0.11mol/L,说明平衡向右移动,该反应是吸热反应,ΔH >0,错误;D、反应达平衡后,再向容器中充入 1 mol PCl5,各组分浓度都变为原来的2倍,增大压强,平衡逆向移动,所以0.1 mol/L<c(Cl2)<0.2 mol/L,正确。
= 1.6×10-3 mol/(L·s),正确;B、平衡时C(Cl2)=0.1mol/L=C(PCl3),C(PCl5)=0.4mo/L,K = 0.025,正确;C升高温度,平衡时c(PCl3)=0.11mol/L,说明平衡向右移动,该反应是吸热反应,ΔH >0,错误;D、反应达平衡后,再向容器中充入 1 mol PCl5,各组分浓度都变为原来的2倍,增大压强,平衡逆向移动,所以0.1 mol/L<c(Cl2)<0.2 mol/L,正确。
考点:考查化学平衡移动、反应速率计算、平衡常数

 考前必练系列答案
考前必练系列答案下列是工业上制取合成氨原料气氢气的一步重要反应:CO(g)+H2O(g)  CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增大压强 | B.降低温度 | C.增大CO的浓度 | D.更换催化剂 |
一定条件下,恒容的密闭容器中,加入一定量的A与B发生反应:A(s)+2B(g) C(g)+2D(g) ΔH<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( )
C(g)+2D(g) ΔH<0,平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( )
| A.增加A的物质的量,正反应速率加快 |
| B.平衡时,其他条件不变,当温度升高时,θ变大 |
| C.图中曲线的斜率表示反应的化学平衡常数 |
| D.平衡时,其他条件不变,再通人B,则反应混合物的温度升高 |
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:
PCl3(g)+ Cl2(g)? PCl5(g);5min末达到平衡,有关数据如右表。
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol?L—1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L—1) | C1 | C2 | 0.4 |
下列判断不正确的是
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5min内,v(PCl3)="0.08" mol?L-1?min-1
C.当容器中为1.2mol时,可逆反应达到平衡状态
D.平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol?L—1
已知:(CH3COOH) 2(g) 2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
| A.该过程的△H<0 |
| B.平衡常数: K(a)=K(b)<K(c) |
| C.气体压强:P(a)<P(b)= P(c) |
| D.当M=80时,(CH3COOH) 2和CH3COOH的物质的量之比为1:1 |
在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1)
2NH3(g) △H=-92.4 kJ·mol-1)
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 4 mol NH3 |
| NH3的浓度(mol·L-1) | c1 | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 气体密度 | ρ1 | ρ2 |
| 反应物转化率 | α1 | α2 |
下列说法正确的是
A.c1<c2<2 c1 B.a+b>92.4 C.α1 +α2=1 D.ρ2=2ρ1
 2C(g),根据下表中的数据判断下列图像错误的是
2C(g),根据下表中的数据判断下列图像错误的是

 2SO2(g)+O2(g)
2SO2(g)+O2(g)
 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是
2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如下图所示。下列说法错误的是