题目内容
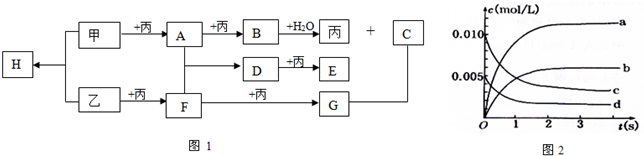
已知甲、乙、丙为常见的单质,A、B、C、D、E、F、G、H均为常见的化合物;B和H的摩尔质量相同,E的相对分子质量比D大16,在一定条件下,各物质相互转化关系如图1所示(产物中水已忽略):
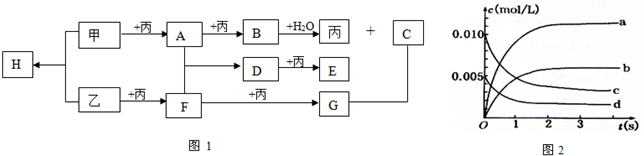
(1)写出下列物质的化学式:丙:______H:______
(2)写出B和F反应的化学方程式:______.
(3)已知25℃,101Kpa时,乙的燃烧热为akJ/mol,写出乙燃烧的热化学方程式______.
(4)写出B+H2O→丙+C的化学方程式______.
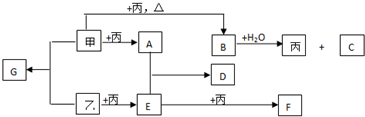
(5)在2L的密闭容器内,500℃时,反应2F(g)+丙(g)═2G(g),n(F)随时间变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(F)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
解:单质甲、乙均能分别与单质丙连续两次反应,可能是单质甲、乙分别被O2连续两次氧化,生成不同的氧化物,则丙是O2.氧化物B与水反应能放出O2,则B是Na2O2,那么C是NaOH,A是Na2O,甲是Na.又因B和H的摩尔质量相同,则H是Na2S,那么乙是S,F是SO2,G是SO3.进一步推出D是Na2SO3,E是Na2SO4,而Na2SO4的相对分子质量比Na2SO3的相对分子质量大16,符合题意,
(1)由以上分析可知丙为O2,H为Na2S,故答案为:O2; Na2S;
(2)B是Na2O2,具有氧化性,F是SO2,具有还原性,二者发生氧化还原反应生成Na2SO4,反应的方程式为
Na2O2+SO2=Na2SO4,
故答案为:Na2O2+SO2=Na2SO4;
(3)乙是S,燃烧热为akJ/mol,燃烧的热化学方程式为S(s)+O2(g)=SO2(g);△H=-akJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-akJ/mol;
(4)B是Na2O2,和水反应生成NaOH和氧气,反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)反应的方程式为:2SO2(g)+O2(g)═2SO3(g),
2s时△n(SO2)=0.020mol/L-0.008mol/L=0.012mol,则生成n(SO3)=0.012mol,浓度为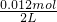 =0.006mol/L,应为b曲线,丙为O2,△n(O2)=0.006mol,则v(O2)=
=0.006mol/L,应为b曲线,丙为O2,△n(O2)=0.006mol,则v(O2)= =0.0015mol?L-1?s-1,
=0.0015mol?L-1?s-1,
故答案为:b;0.0015mol?L-1?s-1.
分析:单质甲、乙均能分别与单质丙连续两次反应,可能是单质甲、乙分别被O2连续两次氧化,生成不同的氧化物,则丙是O2.氧化物B与水反应能放出O2,则B是Na2O2,那么C是NaOH,A是Na2O,甲是Na.又因B和H的摩尔质量相同,则H是Na2S,那么乙是S,F是SO2,G是SO3.进一步推出D是Na2SO3,E是Na2SO4,而Na2SO4的相对分子质量比Na2SO3的相对分子质量大16,符合题意,结合对应物质的性质以及题目要求可解答该题.
点评:本题考查了无机物的推断,侧重于物质转化关系的综合应用、物质性质的应用、反应现象的判断和特征应用,主要是考查物质转化的特征反应和条件判断,掌握常见物质的性质和反应特征、反应条件是解题关键,题目难度中等.
(1)由以上分析可知丙为O2,H为Na2S,故答案为:O2; Na2S;
(2)B是Na2O2,具有氧化性,F是SO2,具有还原性,二者发生氧化还原反应生成Na2SO4,反应的方程式为
Na2O2+SO2=Na2SO4,
故答案为:Na2O2+SO2=Na2SO4;
(3)乙是S,燃烧热为akJ/mol,燃烧的热化学方程式为S(s)+O2(g)=SO2(g);△H=-akJ/mol,
故答案为:S(s)+O2(g)=SO2(g);△H=-akJ/mol;
(4)B是Na2O2,和水反应生成NaOH和氧气,反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)反应的方程式为:2SO2(g)+O2(g)═2SO3(g),
2s时△n(SO2)=0.020mol/L-0.008mol/L=0.012mol,则生成n(SO3)=0.012mol,浓度为
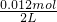 =0.006mol/L,应为b曲线,丙为O2,△n(O2)=0.006mol,则v(O2)=
=0.006mol/L,应为b曲线,丙为O2,△n(O2)=0.006mol,则v(O2)= =0.0015mol?L-1?s-1,
=0.0015mol?L-1?s-1,故答案为:b;0.0015mol?L-1?s-1.
分析:单质甲、乙均能分别与单质丙连续两次反应,可能是单质甲、乙分别被O2连续两次氧化,生成不同的氧化物,则丙是O2.氧化物B与水反应能放出O2,则B是Na2O2,那么C是NaOH,A是Na2O,甲是Na.又因B和H的摩尔质量相同,则H是Na2S,那么乙是S,F是SO2,G是SO3.进一步推出D是Na2SO3,E是Na2SO4,而Na2SO4的相对分子质量比Na2SO3的相对分子质量大16,符合题意,结合对应物质的性质以及题目要求可解答该题.
点评:本题考查了无机物的推断,侧重于物质转化关系的综合应用、物质性质的应用、反应现象的判断和特征应用,主要是考查物质转化的特征反应和条件判断,掌握常见物质的性质和反应特征、反应条件是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目