题目内容
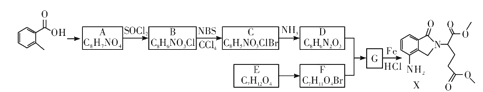
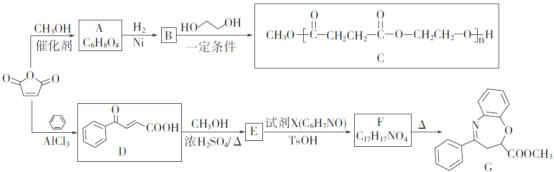
【题目】三种短周期元素x、y、z对应的单质X、Y、Z,常温常压下均为无色气体,在适当条件下单质X、Y、Z之间可以发生如图所示的变化。已知B分子组成中z原子个数比C分子中多一个。

请回答下列问题:
(1)元素x的原子结构示意图___;元素y在周期表中的位置是___;
(2)写出单质氟与C反应的离子反应方程式:___。
(3)Y与X在一定条件下生成化合物A的化学方程式:___。
(4)一定条件下,将盛有10mLA的大试管倒置于水槽的水中然后缓缓通入Y至液体刚好充满试管,写出反应的化学方程式___;通入相同状况下气体Y的体积为___。
(5)用电子式表示B的形成过程___。
【答案】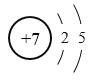 第二周期ⅥA族 2F2+2H2O=4HF+O2 N2+O2
第二周期ⅥA族 2F2+2H2O=4HF+O2 N2+O2![]() 2NO 4NO+3O2+2H2O═4HNO3 7.5mL
2NO 4NO+3O2+2H2O═4HNO3 7.5mL ![]() +3
+3![]()
![]()
![]()
【解析】
三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,则这三种气体是氮气、氧气和氢气(稀有气体除外),生成的三种化合物有NO、H2O、NH3,B分子组成中z原子个数比C分子中多一个,比较这三种分子知,只有水分子中的H原子比氨气分子中的氢原子少一个,所以z为H元素,A分子为NO,B分子为NH3H2O,C分子为H2O,所以y是O元素,x为N元素。
(1)x是N元素,氮原子核外有2个电子层,最外层有5个电子,元素x的原子结构示意图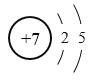 ;y为O元素,氧原子核外有2个电子层,最外层电子数是6元素y在周期表中的位置是第二周期ⅥA族;
;y为O元素,氧原子核外有2个电子层,最外层电子数是6元素y在周期表中的位置是第二周期ⅥA族;
故答案为: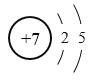 ;第二周期ⅥA族;
;第二周期ⅥA族;
(2)C为水,单质氟与C反应的离子反应方程式:2F2+2H2O=4HF+O2。
故答案为:2F2+2H2O=4HF+O2;
(3)y是O元素,x为N元素,Y与X在一定条件下生成化合物A的化学方程式:N2+O2![]() 2NO;
2NO;
故答案为:N2+O2![]() 2NO;
2NO;
(4)一定条件下,将盛有10mLNO的大试管倒置于水槽的水中然后缓缓通入O2至液体刚好充满试管,反应的化学方程式4NO+3O2+2H2O═4HNO3;由4NO+3O2+2H2O═4HNO3可知,通入相同状况下气体Y的体积为![]() =7.5mL。
=7.5mL。
故答案为:4NO+3O2+2H2O═4HNO3;7.5mL;
(5)B为NH3,三个氢原子和氮原子以共用电子对而形成共价键,其形成过程为:用电子式表示B的形成过程:![]() +3
+3![]()
![]()
![]() 。
。
故答案为: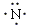 +3
+3![]()
![]()
![]() 。
。

 阅读快车系列答案
阅读快车系列答案