题目内容
某校化学研究性学习小组的同学在学习了氨的性质后,讨论NH3能否还原CuO,设计实验来研究这个问题.(1)①实验室常用加热氯化铵固体和氢氧化钙固体混合物的方法来制取氨气,写出反应的化学方程式:
②实验室还可用
(2)该小组成员设计实验探究氨气的还原性及其产物,实验装置(夹持及尾气处理装置未画出)如图所示.
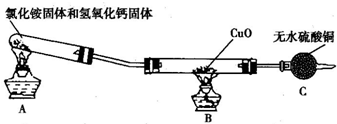
①该装置在设计上有一定的缺陷,为确保实验结果的准确性,你对该装置改进的措施是
②利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体.请写出NH3与CuO反应的化学方程式:
(3)该小组成员用氨气还原氧化铜的方法测定铜的近似相对原子质量,如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下图所示的仪器设计一个简单的实验方案.
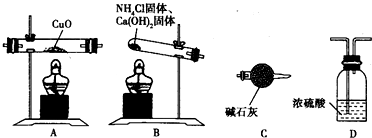
①仪器连接的顺序是
②D中浓硫酸的作用是
③列出计算铜的近似相对原子质量的表达式:
分析:(1)①实验室用固体氯化铵和熟石灰粉末混合加热制取氨气的化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气;
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气污染空气,C装置后需要连接尾气吸收装置,
②由题意可知生成物为铜、氮气和水,以此书写化学方程式;
(3)①根据题给的要求来测量氧化铜和水的质量,考虑到氨气可以和浓硫酸反应,但是不和碱石灰反应,所以应该用碱石灰来吸收水,而用浓硫酸来吸收氨气,可以据此答题;
②氨气可以和硫酸之间发生反应;
③根据化学方程式结合氧化铜和水之间的质量情况进行计算.
| ||
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气;
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气污染空气,C装置后需要连接尾气吸收装置,
②由题意可知生成物为铜、氮气和水,以此书写化学方程式;
(3)①根据题给的要求来测量氧化铜和水的质量,考虑到氨气可以和浓硫酸反应,但是不和碱石灰反应,所以应该用碱石灰来吸收水,而用浓硫酸来吸收氨气,可以据此答题;
②氨气可以和硫酸之间发生反应;
③根据化学方程式结合氧化铜和水之间的质量情况进行计算.
解答:解:(1)①实验室用氯化铵和消石灰反应制备氨气,反应的化学方程式为2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气,故答案为:NaOH固体或生石灰或碱石灰等;
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气污染空气,C装置后需要连接尾气吸收装置,
故答案为:在装置A与B之间增加装有碱石灰的干燥管;C装置之后增加尾气吸收装置;
②根据氨气和氧化铜反应的现象:CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体,说明生成铜、氮气和水,反应的化学方程式为3CuO+2NH3
3Cu+N2+3H2O,故答案为:3CuO+2NH3
3Cu+N2+3H2O;
(3))①根据题给的要求来测量氧化铜和水的质量,考虑到氨气可以和浓硫酸反应,但是不和碱石灰反应,所以应该用碱石灰来吸收水,而用浓硫酸来吸收氨气,由于在制取氨气的过程中要产生水,所以应该先对产生的氨气进行干燥,即选择c装置,然后进行实验,最后为了防止氨气污染空气,所以要用浓硫酸来处理尾气,即正确的操作顺序为:BCACD,故答案为:BCACD;
②浓硫酸可以和氨气之间发生反应,可以用来吸收尾气氨气,防止污染空气,故答案为:进行尾气处理;
③设铜的相对原子质量为x
2NH3+3CuO
N2+3Cu+3H2O
3(x+16)54
m(CuO) m(H2O)
=
解得x=
,故答案为:
.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气,故答案为:NaOH固体或生石灰或碱石灰等;
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气污染空气,C装置后需要连接尾气吸收装置,
故答案为:在装置A与B之间增加装有碱石灰的干燥管;C装置之后增加尾气吸收装置;
②根据氨气和氧化铜反应的现象:CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体,说明生成铜、氮气和水,反应的化学方程式为3CuO+2NH3
| ||
| ||
(3))①根据题给的要求来测量氧化铜和水的质量,考虑到氨气可以和浓硫酸反应,但是不和碱石灰反应,所以应该用碱石灰来吸收水,而用浓硫酸来吸收氨气,由于在制取氨气的过程中要产生水,所以应该先对产生的氨气进行干燥,即选择c装置,然后进行实验,最后为了防止氨气污染空气,所以要用浓硫酸来处理尾气,即正确的操作顺序为:BCACD,故答案为:BCACD;
②浓硫酸可以和氨气之间发生反应,可以用来吸收尾气氨气,防止污染空气,故答案为:进行尾气处理;
③设铜的相对原子质量为x
2NH3+3CuO
| ||
3(x+16)54
m(CuO) m(H2O)
| 3(x+16) |
| m(CuO) |
| 54 |
| m(H2O) |
解得x=
| 18m(CuO) |
| m(H2O) |
| 18m(CuO) |
| m(H2O) |
点评:注意分析题给的条件,知道浓硫酸和碱石灰的作用,为了用纯净、干燥的氨气还原氧化铜,并通过测定生成水的质量来测铜的相对原子质量,要注意先除去氨气中的杂质,即除去水.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
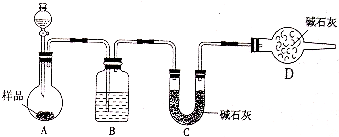

 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.