题目内容
【题目】已知甲基丙烯酸缩水甘油酯(GMA)主要用于高分子胶囊、离子交换树脂和印刷油墨的粘合剂。其合成路线如下:

请回答下列问题:
(1)GMA中的官能团名称是_________________________________。
(2)甘油的结构简式是___________,F的结构简式___________。
(3)请写出B→C、D→E的化学方程式,并判断反应类型:
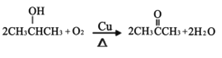
B→C:_________________________________、___________反应;
D→E:_________________________________、___________反应。
(4)E的核磁共振氢谱峰面积之比由大到小为___________,E的同分异构体中能发生水解反应的链状化合物有___________种。
(5)已知CH2=CH2能在Ag作催化剂的条件下与O2反应生成![]() ,据此请设计一条由丙烯生成F的路线。____________________________________________。
,据此请设计一条由丙烯生成F的路线。____________________________________________。
【答案】碳碳双键、酯基和醚键 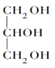
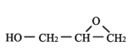
 氧化
氧化 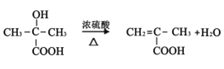 消去 3:2:1 5
消去 3:2:1 5 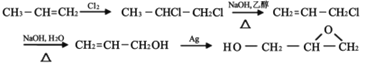
【解析】
由GMA结构简式和题给框图可知,丙烯(CH3CH=CH2)与HCl发生加成反应生成CH3CH(Cl)CH3,则A为CH3CH(Cl)CH3;CH3CH(Cl)CH3在氢氧化钠溶液中加热发生水解反应生成CH3CH(OH)CH3,CH3CH(OH)CH3发生催化氧化反应生成![]() ,则C为
,则C为![]() ;
;![]() 发生信息反应生成
发生信息反应生成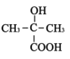 ,则D为
,则D为 ;
; 在浓硫酸加热条件下发生消去反应生成
在浓硫酸加热条件下发生消去反应生成![]() ,则E为
,则E为![]() ;由E和GMA结构简式可知,F为
;由E和GMA结构简式可知,F为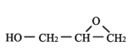 。
。
(1)GMA结构简式为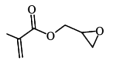 ,其含有的官能团为碳碳双键、酯基和醚键,故答案为:碳碳双键、酯基和醚键;
,其含有的官能团为碳碳双键、酯基和醚键,故答案为:碳碳双键、酯基和醚键;
(2)甘油为丙三醇,结构简式是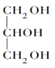 ;由E和GMA结构简式可知,F为
;由E和GMA结构简式可知,F为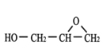 ,故答案为:
,故答案为: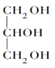 ;
;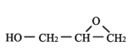 ;
;
(3)B→C的反应为CH3CH(OH)CH3发生催化氧化反应生成![]() ,反应的化学方程式为
,反应的化学方程式为 ;D→E的反应为
;D→E的反应为 在浓硫酸加热条件下发生消去反应生成
在浓硫酸加热条件下发生消去反应生成![]() ,反应的化学方程式为
,反应的化学方程式为 ,故答案为:
,故答案为: ;氧化;
;氧化; ;消去;
;消去;
(4)E为![]() ,其核子共振氢谱有3组峰,面积为3:2:1;E的同分异构体中能发生水解反应的链状化合物应为酯,可能为甲酸酯、乙酸酯和丙烯酸酯,若为甲酸酯有3种、若为乙酸酯有1种、若为丙烯酸酯有1种,共有5种,故答案为:3:2:1;5;
,其核子共振氢谱有3组峰,面积为3:2:1;E的同分异构体中能发生水解反应的链状化合物应为酯,可能为甲酸酯、乙酸酯和丙烯酸酯,若为甲酸酯有3种、若为乙酸酯有1种、若为丙烯酸酯有1种,共有5种,故答案为:3:2:1;5;
(5)结合题给信息,由逆推法可知丙烯生成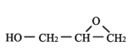 的合成步骤为:丙烯(CH3CH=CH2)与氯气发生加成反应生成
的合成步骤为:丙烯(CH3CH=CH2)与氯气发生加成反应生成![]() ,
,![]() 在氢氧化钠醇溶液中发生消去反应生成
在氢氧化钠醇溶液中发生消去反应生成![]() ,
,![]() 在氢氧化钠溶液中加热发生水解反应生成
在氢氧化钠溶液中加热发生水解反应生成![]() ,
,![]() 在Ag作催化剂的条件下与O2反应生成
在Ag作催化剂的条件下与O2反应生成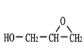 ,合成路线为:
,合成路线为: ,故答案为:
,故答案为: 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列说法正确的是
A.乙酸、葡萄糖都可用通式Cn(H2O)m表示其组成,所以乙酸也属于糖类
B.凡是能溶于水且具有甜味的化合物都属于糖类
C.蔗糖能发生银镜反应
D.葡萄糖分子中含有醛基,它具有还原性
【题目】元素的性质随原子序数的递增呈周期性变化的原因是( )
A. 元素原子的核外电子排布呈周期性变化 B. 元素原子的电子层数呈周期性变化
C. 元素的化合价呈周期性变化 D. 元素原子半径呈周期性变化
【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
温 度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应为_____ (填放热,吸热,无法确定 )反应。
②下列措施能用勒夏特列原理解释是_____(填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应式_____。
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl﹣),则一水合氨的电离平衡常数Kb=_____(用ab表示)。
(4)原料气H2可通过反应 CH4(g)+H2O (g)![]() CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的![]() 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
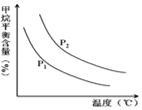
①图中,两条曲线表示压强的关系是:P1_____P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会__(填“增大”,“减小”减小,“不变”不变)。
(5)原料气H2还可通过反应CO(g)+H2O(g)![]() CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08molL﹣1,该温度下反应的平衡常数K值为_____。
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是_____(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6





