题目内容
6.氢氟酸是一种弱酸,可用来刻蚀玻璃.已知25℃时:①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H=-67.7kJ•mol-1②H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1氢氟酸的电离方程式及热效应可表示为:HF(aq)?H+(aq)+F-(aq)△H=-10.4kJ•mol-1.分析 先写出目标反应的热化学方程式,然后根据盖斯定律及已知热化学方程式,通过①-②可得目标反应的热化学方程式.
解答 解:①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H=-67.7kJ•mol-1,
②H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,
结合盖斯定律①-②得到:HF(aq)?H+(aq)+F-(aq)△H=-10.4kJ•mol-1,
故答案为:HF(aq)?H+(aq)+F-(aq)△H=-10.4kJ•mol-1.
点评 本题考查了盖斯定律在书写热化学方程式中的应用,题目难度中等,明确盖斯定律的含义为解答关键,注意熟练掌握热化学方程式的书写原则,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
17.现有盐酸、新制氯水、NaCl溶液和NaOH溶液,可用一种试剂将它们一一区别开,该试剂是( )
| A. | AgNO3溶液 | B. | 酚酞试液 | C. | 紫色石蕊试液 | D. | 饱和NaCl溶液 |
14.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3 g的Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA | |
| C. | 1.0 L的0.1 mol•L-1Na2S溶液中含有的S2-数为0.1NA | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
1.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A. | K+、Na+、HCO3-、NO3- | B. | Ag+、K+、NO3-、Na+ | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Na+、SO42-、Cl-、ClO- |
18.国际上推广使用中国铁锅,这是因为铁锅( )
| A. | 是单质 | B. | 含碳,属混合物 | ||
| C. | 化学性质活泼 | D. | 易使食物中含人体所需的铁元素 |
15.以下能级符号正确的是( )
| A. | 5s | B. | 2d | C. | 3 f | D. | 1p |
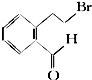 下面的框图是应用2-(2-溴乙基)苯甲醛为原料合成有机化合物C和F的流程图:
下面的框图是应用2-(2-溴乙基)苯甲醛为原料合成有机化合物C和F的流程图: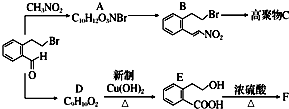
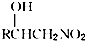
 .
.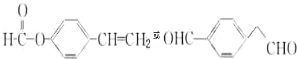 .
.