题目内容
【题目】对氮、碳及其化合物的研究具有重要意义。
(1)用肼(N2H4)为燃料,四氧化二氮做氧化剂,两者反应生成氮气和气态水。
已知:N2(g)+2O2(g)=N2O4(g)△H1K1
N2H4(g)+O2(g)=N2(g)2H2O(g)△H2K2
则2N2H4(g)+ N2O4(g)=3N2(g)+ 4H2O(g) △H= (用△H1、△H2表示),该反应的化学平衡常数K = (用K1、K2表示)
(2)汽车尾气转化反应:NO+CO→N2+CO2(未配平),将NO和CO转化为和N2和CO2,实现除污,每生成1molN2还原剂失去电子数为 。
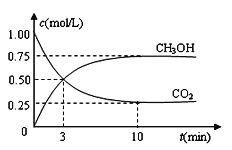
(3) 大气污染物氮氧化物可以用活性炭还原法处理。某研究小组向某2L的密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2 (g)。在T1℃时,反应进行到不同时间(t)测得各物质的物质的量(n)如下
N2(g)+CO2 (g)。在T1℃时,反应进行到不同时间(t)测得各物质的物质的量(n)如下
t(min) n(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 2.00 | 1.16 | 0.80 | 0.80 | 0.96 | 0.96 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
CO2 | 0 | 0.42 | 0.60 | 0.60 | 0.72 | 0.72 |
0~10min内,NO的平均反应速率v(NO)= ;T1℃时,该反应的平均常数K= 。
②30min后,只改变某一条件,反应重新达到平衡,根据上表的数据判断改变的条件可能是 (填字母编号)。
a.加入一定量的活性炭 b.通入一定量的NO
c.恒温时,充入一定量的氦气 d.加入适量的催化剂
(4)氨燃料电池使用的电解质溶液是2mol·L-1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O,放电时,该电池正极的电极反应式为 。
(5)不能作为判断反应达到化学平衡状态的依据是 (填字母序号)。
A.容器内CO2的浓度保持不变
B.v正(N2)=2v逆(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
【答案】(1)2△H2—△H1(1分) K22/K1(1分)
(2)4NA或4×6.02X1023(2分)
(3)①0.042mol·L-1·min-1(2分) 0.56(或9/16)(2分) ②b(1分)
(4)O2+2H2O+4e-=4OH-(2分)
(5)BC(2分)
【解析】
试题分析:(1)已知:①N2(g)+2O2(g)=N2O4(g)△H1
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2
根据盖斯定律,②×2-①可得:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),则△H=2△H2-△H1,该反应平衡常数K=K22/K1;
(2)反应中N元素化合价由+2价降低为0价,每生成1molN2还原剂失去电子数为1mol×4×6.02×1023mol-1=4×6.02×1023;
(3)①①0~10min内,NO的平均反应速率v(NO)=![]() =0.042mol/(L.min);
=0.042mol/(L.min);
由表中数据可知,20min时处于平衡状态,反应前后气体的体积不变,用物质的量代替浓度计算平衡常数,则K=![]() =9/16;②反应重新达到平衡,NO增大0.16mol,N2、CO2 均增大0.08mol,等于化学计量数之比,应是通入一定量的NO,故选b;
=9/16;②反应重新达到平衡,NO增大0.16mol,N2、CO2 均增大0.08mol,等于化学计量数之比,应是通入一定量的NO,故选b;
(4)氨燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O.放电时,正极发生还原反应,氧气在正极获得电子,碱性条件下生成氢氧根离子,正极电极反应式为:O2+2H2O+4e-=4OH-;
(5)A.容器内CO2的浓度保持不变,可判断反应达到平衡状态,故A正确; B.v正(N2)=2v逆(NO),两速率比不等于化学计量数之比,反应没有达到平衡状态,故B正确;C.反应体系,气态反应物与气态生成物系数和相等,容器内压强保持不变,无法判断反应达到平衡状态,故C错误;D.反应体系中C为固体,则混合气体的密度保持不变,可知反应达到平衡状态,故C正确;E.反应体系中C为固体,气态反应物与气态生成物系数和相等,则混合气体的平均相对分子质量保持不变,可推知反应达到平衡状态,故E正确,答案为BC。