��Ŀ����
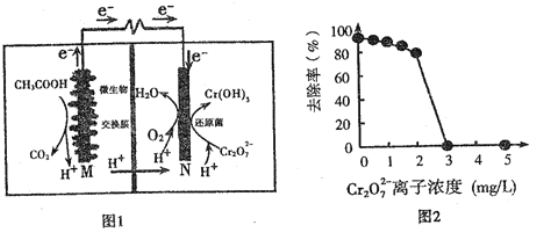
����Ŀ����ͼ��ʾ��p��qΪֱ����Դ��������A�ɽ�������X�Ƴɣ�B��C��DΪ���缫����ͨ��Դ������X������B����ͬʱC��D�ϲ������ݣ��Իش� 
��1��pΪ����A����������Ӧ��
��2��CΪ�������ռ�����DΪ�������ռ��� ��
��3��C���ĵ缫��ӦʽΪ ��
��4���ڵ������У���C��D�����ϲ�������������ʵ�����������
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
������������������cm3�� | 6 | 12 | 20 | 29 | 39] | 49 | 59 | 69 | 79 | 89 |
������������������cm3�� | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
��ϸ��������ʵ�����ݣ���˵���仯�Ŀ���ԭ���� ��
��5������Ӧ����һ��ʱ���A��B�缫������Һ��pH���������С�����䡱����
��6������·��ͨ��0.004mol����ʱ��B���ϳ����Ľ���XΪ0.128g����˽�����Ħ������Ϊ ��
���𰸡�
��1����������
��2��������������������
��3��4OH����4e��=O2��+2H2O
��4����ʼʱC��D�������������Ϊ1��3,10����ʱԼΪ1��2,˵����ʼʱ�����ܽ�����Һ��
��5������
��6��64g/mol
���������⣺��1����ͨ��Դ������X������B����ͬʱC��D�������ݣ���BΪ������X�����������ŵ����ɽ������ʣ���A��C��������B��D������������p��������A�缫��ʧ���ӷ���������Ӧ��
�ʴ�Ϊ��������������2��C�缫�ǵ������������������������ӷŵ磻DΪ���������ӷŵ������������ʴ�Ϊ������������������������3��C�����������������������ӷŵ������������缫��ӦʽΪ��4OH����4e��=O2��+2H2O��
�ʴ�Ϊ��4OH����4e��=O2��+2H2O����4��������������������ˮ������������������ˮ������1��6�����������������ܽ�Ŀ���࣬�Ӷ������������������ɵ��������֮�ȴ���2��1��
�ʴ�Ϊ����ʼʱC��D�������������Ϊ1��3��10����ʱԼΪ1��2��˵����ʼʱ�����ܽ�����Һ�У���5�����������Һʵ���ϵ�����ˮ�����һ��ʱ���A��B�缫������Һ��pH���䣬�ʴ�Ϊ�����䣻��6������Ħ������ΪM�����ʱ��B�缫�ϵĵ缫��ӦʽΪX 2++2e��=X����
X2++ | 2e��= | X |
2mol | 1mol | |
0.004mol |
|
��M= ![]() =64g/mol��
=64g/mol��
�ʴ�Ϊ��64g/mol��
��1����ͨ��Դ������X������B����ͬʱC��D�������ݣ���BΪ������X�����������ŵ����ɽ������ʣ���A��C��������B��D�������������������ǵ�Դ��������2��C�缫�ǵ������������������������ӷŵ磻DΪ���������ӷŵ�������������3�����ݵ��ԭ���ڹ�ҵ�ϵ�Ӧ��֪ʶ���ش𣻣�4�������������������ܽ��Ժ��ܽ�ȵȷ�����з�������5�����ݷ����������ʷ�������6�����ݽ�����ת�Ƶ���֮��Ĺ�ϵʽ���㣮

 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д� Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�