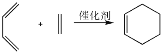��Ŀ����
����Ŀ�����и���˵��������ȷ���ǣ� ��
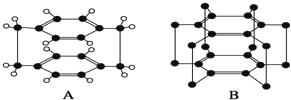
��CH3��CH��CH��C��C��CF3 ���ӽṹ������� 4 ��̼ԭ����һ��ֱ����
���ô�����ķ����ɳ�ȥ�����л��е�������ϩ
�۶���ϩ�Ͷ�ϩΪͬϵ��
�������顢�����顢������ķе����
��14 g ��ϩ�ͱ�ϩ��������е���ԭ����Ϊ 2NA
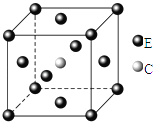
���ܹ����١�������ȷ�IJⶨ��Է������������������Ǻ˴Ź�������
A.�ڢۢ�B.�٢ۢ�C.�ڢۢ�D.�ۢܢ�
���𰸡�A
��������
��̼̼������ֱ�ߣ�̼̼˫����ƽ�棬�������������Ĵ���ʹCH3��CH��CH��C��C��CF3 ���ӽṹ������� 4 ��̼ԭ����һ��ֱ���ϣ�����ȷ��
�������ǹ�����,���Եõ��������к�������,�Dz����ģ���ȷ�����ǽ��������ͨ����ˮ�����, �ڴ���
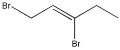
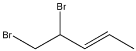
�۽ṹ���ƣ��ڷ�����������һ�������ɸ�CH2ԭ���ŵ����ʻ���Ϊͬϵ�����ϩ������̼̼˫������ϩֻ��һ�������Խṹ��ͬ���۴���
����Է���������ͬ��ͬ���칹�壬һ����֧��Խ�࣬�۷е�Խ�ͣ������顢�����顢������ķе���ͣ�����ȷ��
����ϩ�ͱ�ϩ�����ʽ��ΪCH2����14 g ��ϩ�ͱ�ϩ�к���CH2Ϊ![]() =1mol��������ԭ����Ϊ 2NA������ȷ��
=1mol��������ԭ����Ϊ 2NA������ȷ��
�˴Ź��������ⶨ������ԭ�ӵ��������Ŀ�������ⶨ��Է�������������
�ʴ�����Тڢۢޡ�
��ѡA��

����Ŀ����Ԫ�ؿ��γɶ��ֻ�����ڹ�ҵ�����о�����Ҫ��ֵ����ش��������⣺
(1)һ���¶��£���һ������N2��H2����̶�������ܱ������н��кϳɰ���Ӧ��
������������˵���ÿ��淴Ӧ�ﵽ��ѧƽ��״̬����__��
A.������������ܶȲ���
B.c(N2)��c(H2)��c(NH3)=1��3��2
C.�����ڵ�ѹǿ����
D.��ͬʱ������3molH-H�����ѣ���6molN-H���γ�
E.3v��(H2)=2v��(NH3)
F.�����������ƽ����Է�����������
�ں��º�ѹ�����£�Ϊ��ߺϳɰ���Ӧ��N2��H2�������ʣ��ɲ��õķ���__(һ�ּ���)��
(2)һ���¶��£�2L�ܱ������г���0.40molN2O4��������Ӧ��N2O4(g)![]() 2NO2(g)��һ��ʱ���ﵽƽ�⣬����������£�
2NO2(g)��һ��ʱ���ﵽƽ�⣬����������£�
ʱ��/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
��20s�ڣ�v(NO2)=__�����¶��·�Ӧ�Ļ�ѧƽ�ⳣ����ֵΪ__��
�������¶�ʱ��������ɫ���������Ӧ��__(��������������������)��Ӧ��
����ͬ�¶��£�����ʼ��������г���0.40mo1NO2����ﵽƽ���c(NO2)__0.15mol/L(����>������=������<��)