题目内容
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
实验目的:制取乙酸乙酯
实验原理:甲、乙、丙三位同学均采用乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是___、___。
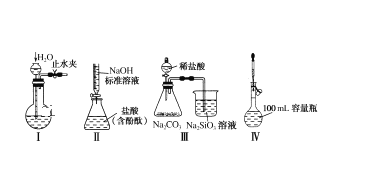
装置设计:甲、乙、丙三位同学分别设计了如图所示三套实验装置:

请从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,应选择的装置是___(填“Ⅰ”或“Ⅱ”)。丙同学将Ⅰ装置中的玻璃导管改成了球形干燥管,除起冷凝作用外,另一重要作用是___。
实验步骤:(1)按选择的装置组装仪器,在试管①中先加入3mL乙醇和2mL冰醋酸,并在摇动下缓缓加入2mL浓硫酸,加入2~3块碎瓷片;
(2)将试管固定在铁架上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验。
问题讨论:a.步骤(1)中组装好实验装置,加入样品前还应检查___。
b.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有___。
c.试管②中饱和Na2CO3溶液的作用是___、___、___。
d.从试管②中分离出乙酸乙酯的实验操作是___。
【答案】催化剂 吸水剂 Ⅱ 防止倒吸 装置的气密性 无色、不溶于水、密度比水小等 溶解乙醇 中和乙酸 降低乙酸乙酯的溶解度 分液
【解析】
实验室用乙醇、乙酸在浓硫酸的催化作用下发生酯化反应制取乙酸乙酯,浓硫酸作催化剂和吸水剂。该实验中由于酒精灯加热可能使其受热不均匀,若导管插入液面以下有可能发生倒吸,所以装置要能防止倒吸。由于乙酸乙酯、乙酸、乙醇的沸点都较低,加热时都能挥发出来,用饱和![]() 溶液可以除去乙酸乙酯中的乙醇和乙酸,在试管②的上层可得到乙酸乙酯油状液体,再经分液漏斗分液即可分离出。
溶液可以除去乙酸乙酯中的乙醇和乙酸,在试管②的上层可得到乙酸乙酯油状液体,再经分液漏斗分液即可分离出。
实验原理:实验室用乙醇、乙酸在浓硫酸的催化作用下发生酯化反应制取乙酸乙酯,浓硫酸作催化剂和吸水剂,故答案为:催化剂;吸水剂;
装置设计:实验中由于酒精灯加热可能使其受热不均匀,若导管插入液面以下有可能发生倒吸,所以装置要能防止倒吸,则选择装置Ⅱ,改成了球形干燥管除了起冷凝作用外还可以防止倒吸,故答案为:Ⅱ;防止倒吸;
问题讨论:a. 由于乙酸乙酯、乙酸、乙醇的沸点都较低,加热时都能挥发出来,所以在进行实验时,组装好实验装置后需要先检查装置气密性,再添加药品开始实验,故答案为:检查装置气密性;
b. 试管②中观察的现象为,溶液分层,上层无色油状液体,故答案为:无色、不溶于水、密度比水小;
c. 由于乙酸乙酯在Na2CO3溶液中的溶解度很小,乙醇可以溶解在Na2CO3中,且Na2CO3显碱性,乙酸可以与Na2CO3发生复分解反应得到乙酸钠和CO2,则饱和Na2CO3的作用为溶解乙醇,反应乙酸,降低乙酸乙酯的溶解度,故答案为:溶解乙醇;中和乙酸;降低乙酸乙酯的溶解度;
d.因为乙酸乙酯与H2O不互溶,可采用分液的方法进行分离,故答案为:分液。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案