题目内容
【题目】Ⅰ.选择合适的图象,用字母填空:
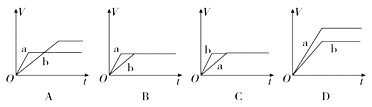
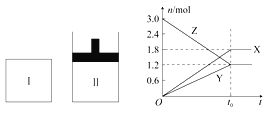
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系的图像是_______。
(2)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是_______。
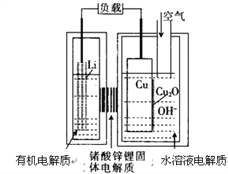
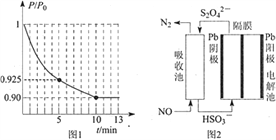
Ⅱ.Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的高效水处理剂,其电解制法如下图所示。电解过程中,两极均有气体产生,Y极区域溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍澄清。查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
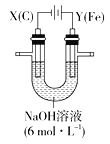
(3)电解过程中,X极区溶液的pH______(填“增大”“减小”或“不变”)。
(4)电解过程中,Y极发生的电极反应为___________和_____________。
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少__________g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2。该电池正极的电极反应式为______________________。
【答案】 A C 增大 Fe-6e-+8OH-===FeO42-+4H2O 4OH--4e-===2H2O+O2↑ 0.28 2FeO42-+6e-+5H2O=Fe2O3+10 OH-
【解析】(1)向a中加入少量的CuSO4溶液,锌置换出铜,构成原电池加快反应速率,但由于消耗锌,产生氢气的体积减少,所以产生H2的体积V(L)与时间t(min)的关系的图像是A。(2)将(1)中的CuSO4溶液改成CH3COONa溶液,醋酸根结合氢离子,降低氢离子浓度,反应速率减小,但最终产生氢气的体积不变,因此图象是C。(3)电解过程中,X极与电源的负极相连,作阴极,氢离子放电,所以X极区溶液的pH增大。(4)电解过程中,Y极与电源的正极相连,作阳极,铁失去电子转化为高铁酸根离子,同时氢氧根也可以放电,所以发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O、4OH--4e-=2H2O+O2↑。(5)若在X极收集到672 mL气体,即氢气是0.03mol。在Y极收集到168 mL气体,即氧气是0.0075mol,则根据电子得失守恒可知消耗铁的物质的量是![]() ,所以Y电极(铁电极)质量减少0.005mol×56g/mol=0.28g。(6)原电池中正极发生得到电子的还原反应,根据总反应式可知正极是高铁酸钾得到电子,该电池正极的电极反应式为2FeO42-+6e-+5H2O=Fe2O3+10OH-。
,所以Y电极(铁电极)质量减少0.005mol×56g/mol=0.28g。(6)原电池中正极发生得到电子的还原反应,根据总反应式可知正极是高铁酸钾得到电子,该电池正极的电极反应式为2FeO42-+6e-+5H2O=Fe2O3+10OH-。

 53随堂测系列答案
53随堂测系列答案【题目】草酸铁晶体Fe2(C2O4)3·xH2O通过相关处理后可溶于水,且能做净水剂,在110℃可完全失去结晶水。为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250 mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根
恰好全部氧化成二氧化碳,同时MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤3:用0.0200 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1 mL,滴定中MnO4-被还原成Mn2+。
重复步骤2、步骤3的操作2次,分别滴定消耗0.0200 mol·L-1 KMnO4溶液为V2、V3 mL。
记录数据如下表:
实验编号 | KMnO4溶液的浓度(mol·L-1) | KMnO4溶液滴入的体积(mL) |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V2 = 20.12 |
3 | 0.0200 | V3 = 19.98 |
请回答下列问题:
(1)草酸铁溶液能做净水剂的原因_________________(用离子方程式表示)
(2)该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的______________ (填序号)
酸式滴定管 B.碱式滴定管 C.量筒(10 mL) D.锥形瓶
E.胶头滴管 F.漏斗 G.250 mL容量瓶
(3)加入锌粉的目的是______________________
(4)步骤3滴定时是否选择指示剂_________(是或否);说明理由_________________________写出步骤3中发生反应的离子方程式____________________________
(5)在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量________(填“偏低”、“偏高”或“不变”);实验测得该晶体中结晶水的个数x为________。