题目内容
(8分)
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
:(1)5;(2)2NH3+NaClO=N2H4+NaCl+H2O;(3)2N2H4(l)+ N2O4(l)="3" N2(g)+ 4H2O(g) △H=-1048.9kJ/mol;(4)N2H4+ 4OH--4e- =4H2O +N2↑。
:(1)氮原子的L层是第二层,该层上的电子数为5;(2)根据题目给出的反应物和部分生成物,分析反应中的化合价变化,NH3转化为N2H4时化合价由-3升高到-2,故NaClO中的氯元素化合价只能下降到-1,可知产物中有NaCl,再结合元素守恒可知一定有水生成,故可表示为:2NH3+NaClO=N2H4+ NaCl +H2O;(3)分析题给方程式,可知由2×②-①得到要求的热化学方程式,故△H=2△H2-△H1,写出结果:2N2H4(l)+ N2O4(l)="3" N2(g)+ 4H2O(g) △H="-1048.9kJ" /mol;(4)碱性电池中负极反应是还原反应,也就是还原剂失电子的反应,结合电解质溶液为碱性条件,故写为:N2H4+ 4OH--4e- =4H2O +N2↑。
【考点定位】此题以氮元素为载体,综合考查了电子层排布、化学方程式书写、盖斯定律的应用、原电池中电极反应式的书写等知识。
【考点定位】此题以氮元素为载体,综合考查了电子层排布、化学方程式书写、盖斯定律的应用、原电池中电极反应式的书写等知识。

练习册系列答案
相关题目

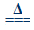 2Ag2O+4NO2↑+O2↑ (Ⅱ)2AgNO3
2Ag2O+4NO2↑+O2↑ (Ⅱ)2AgNO3

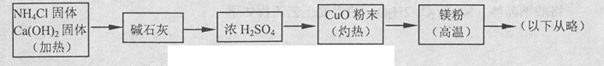
 3Cu+N2+3H2O),而氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水立即反应生成Mg(OH)2和NH3。乙组提出了如下制备氮化镁的实验方案示意框图(实验前系统内空气已排除;图中箭头表示气体的流向)。你认为此方案是否正确,并说明理由 。
3Cu+N2+3H2O),而氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水立即反应生成Mg(OH)2和NH3。乙组提出了如下制备氮化镁的实验方案示意框图(实验前系统内空气已排除;图中箭头表示气体的流向)。你认为此方案是否正确,并说明理由 。