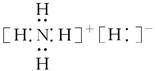题目内容
三氟化氮(NF3)是一种无色无味的气体,它是氨(NH3)和氟(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F 。下列有关NF3的叙述正确的是
| A.NF3是离子化合物 | B.NF3分子构型是平面三角形 |
| C.NF3的氧化性比F2强 | D.NF3中的N呈+3价 |
D
试题分析:A.NF3是共价化合物。错误。B.NF3分子构型是三角锥形。错误。C.氧化性比F2比NF3的强。错误。D.由于非金属性F>N。所以共价化合物中正负化合价的代数和为0 的原子,在化合物NF3中的N呈+3价。正确。 3的分子结构与性质的知识。

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目